Fármacos: la vida en equilibrio
La combinación de dos o más medicamentos puede ser una herramienta importante para el estudio de los sistemas biológicos y revelar relaciones respecto a los diferentes procesos celulares. Las interacciones entre dos fármacos se pueden clasificar como aditivas, sinérgicas o antagónicas de acuerdo a si su efecto combinado es igual, mayor o menor que lo esperado sobre la base de sus efectos individuales. Se ha prestado mucha atención a las combinaciones de medicamentos sinérgicos debido a su gran potencialidad. El antagonismo, sin embargo, podría tener una ventaja al retrasar e incluso invertir la evolución de la resistencia. Una especie particularmente fuerte de antagonismo, denominada "supresión", ocurre cuando el efecto combinado de dos drogas inhibidoras no sólo es más débil que la suma esperada, sino que también más débil que el resultado de un solo fármaco.
Principio de equilibrio para las interacciones entre fármacos
La terapia de combinación de drogas - la administración simultánea de más de un medicamento para tratar una sola enfermedad - tiene diversas aplicaciones, incluyendo el manejo de infecciones microbianas, virales y el cáncer. El diseño de nuevas asociaciones terapéuticas, sin embargo, puede ser un gran desafío, porque los fármacos a menudo interactúan de manera no trivial. Incluso, una simple combinación puede producir resultados diversos. La sinergia, más eficaz a través de la suma de los efectos individuales de sus componentes, es altamente esperada, ya que a menudo requiere una reducción de las dosis administradas. Pero las combinaciones medicamentosas también pueden ser antagónicas o incluso supresivas, lo que lleva a casos en que el resultado combinado es más débil que la de cada uno de los fármacos de forma aislada. Una mejor comprensión de cómo surgen tales efectos beneficiaría el desarrollo racional de las terapias combinadas.
Un estudio realizado por Tobias Bollenbach y colaboradores (Cell 2009; 139:707-718) abarca el tema. Los investigadores habían observado previamente una inusual interacción de supresión mientras cuantificaban los efectos de las combinaciones de dos medicamentos en el crecimiento de Escherichia coli. El efecto de los antibióticos anticrecimiento de una clase de inhibidores de la síntesis de ADN se revirtió parcialmente cuando se combinaron con principios de segunda clase, inhibidores de la síntesis de proteínas. Esta observación sugiere una hipótesis mecanicista, en términos de recursos y condiciones óptimas para el crecimiento, mediante modelos matemáticos y análisis con una serie de experimentos cuantitativos.
El grupo de T. Bollenbach obtuvo una simple explicación para la supresión. Cuando los inhibidores de la síntesis de ADN se administran a las bacterias, el equilibrio óptimo entre los niveles de proteínas y ADN en las células se inclina hacia un alto nivel de proteínas. La regulación decreciente de la síntesis ribosomal en respuesta al estrés del ADN podría corregir el desequilibrio mediante la reducción de la síntesis proteica. Sin embargo, como lo demostrado en experimentos de transcripción, estas células tienen la capacidad para llevar a cabo tal regulación. Sin embargo, añadir un segundo antibiótico que inhiba la síntesis de proteínas puede restaurar el equilibrio entre el ADN y las proteínas, lo que implica una utilización más equilibrada de los recursos metabólicos y celulares que conduzcan a la recuperación del ritmo de crecimiento - lo contrario de lo que cabría esperar (figura 1).
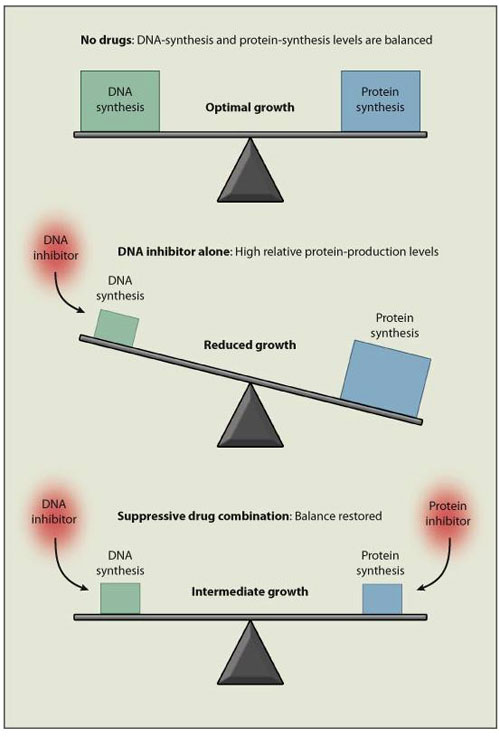
El efecto supresor que los inhibidores antibióticos de la síntesis de proteínas tienen sobre los inhibidores de la síntesis de ADN se muestra en la base del equilibrio del sistema, según T. Bollenbach y colegas. Aunque un inhibidor de la síntesis de ADN altera el equilibrio óptimo intracelular entre la síntesis de ADN y la producción de proteínas hacia niveles excesivamente altos de proteínas, el balance puede ser restaurado por un inhibidor de la síntesis proteica, provocando la inhibición de las drogas.
Una nueva y atractiva forma para la interpretación de las interacciones medicamentosas (incluso más allá de los sistemas microbianos) es que el óptimo funcionamiento celular fisiológico dependa del trastorno intracelular y que las drogas puedan alteran ese equilibrio, más que afectar la salida de una vía. En el cáncer, es bien sabido que medicamentos de diferentes clases que actúan en varias vías se pueden potenciar recíprocamente de forma aditiva o sinérgica cuando se utilizan en combinación. Por lo general no se sabe cómo el equilibrio celular podría verse afectado por la acción de cada medicamento, un área potencialmente interesante para la investigación.
Los biólogos del cáncer podrían descubrir situaciones en las que la acción individual de dos o más medicamentos alteraría el mismo equilibrio fisiológico celular de forma complementaria, de modo que su combinación restaure el equilibrio y por lo menos en parte, invierta el efecto terapéutico de un solo medicamento. Este tipo de combinaciones debería ser evitado. En el lado positivo, las interacciones de supresión pueden ser una herramienta para investigar de forma sistemática los mecanismos que regulan el equilibrio intracelular y su efecto sobre el estado de las células, como el crecimiento o la diferenciación. Para beneficio clínico, uno puede ser capaz de explotar el principio de equilibrio y racionalidad del diseño combinaciones de fármacos que alteran el equilibrio de forma sinérgica. La sinergia dual puede ser posible cuando los dos fármacos afectan diferentes vías y al desequilibrio de la función fisiológica general. Así, con buenos datos cuantitativos y modelos matemáticos predictivos en mano, se puede esperar encontrar nuevas terapias que tengan en cuenta los balances celulares y de forma irreversible y sinérgicamente, alterarlos para un determinado efecto terapéutico deseado.
En las infecciones microbianas, así como en el cáncer, la atención se ha centrado en el descubrimiento directo de las interacciones medicamentosas sinérgicas. El estudio de T. Bollenbach y colegas sugiere que otros aspectos de la interacción merecen ser estudiados, al igual que sus trabajos anteriores que indican que la combinación antagónica puede reducir la resistencia de los medicamentos y por lo tanto ser ventajosa cuando existe la amenaza de resistencia. Surge un principio general respecto al efecto que las interacciones medicamentosas no triviales pueden tener en los equilibrios globales básicos de la fisiología celular. La aplicación de este principio podría guiarnos con más fuerza para evitar los efectos inesperados y para el diseño de combinaciones sinérgicas que puedan tratar una variedad de enfermedades infecciones microbianas.
Fuente bibliográfica
Principle of System Balance for Drug Interactions
Xavier JB, Sander C.
Computational Biology Center, Memorial Sloan-Kettering Cancer Center, New York, USA.
N Engl J Med. 2010 Apr 8; 362(14):1339-40