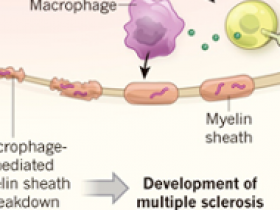
Autoproliferación inmune y esclerosis múltiple
La esclerosis múltiple es una enfermedad autoinmune causada por la interacción de factores genéticos, particularmente el haplotipo HLA-DR15, y factores de riesgo ambientales. Sin embargo, no está claro cómo estos componentes etiológicos contribuyen a generar un repertorio de células T CD4+ autorreactivas. Recientemente, se demostró que la autorreactividad, definida como "autoproliferación" de células Th1 periféricas, es elevada en pacientes portadores del haplotipo HLA-DR15. La autoproliferación está mediada por células B de memoria de una manera dependiente de HLA-DR. Además, se observa que el agotamiento de linfocitos B in vitro y terapéuticamente in vivo vía anti-CD20 reduce eficazmente la autoproliferación de células T. Estos hallazgos serán decisivos para abordar las interacciones patogénicas entre los linfocitos T y B en la esclerosis múltiple, y también para desarrollar nuevas terapias.
Proteína RASGRP2
Una característica distintiva de la esclerosis múltiple es un ataque autoinmune inflamatorio sobre las proteínas de la vaina de mielina, una estructura que se extiende alrededor de las fibras nerviosas que se proyectan desde las neuronas. La vaina de mielina proporciona protección y nutrición a las fibras nerviosas y permite una transmisión eficaz de los impulsos nerviosos. La lesión de la vaina de mielina causa una variedad de síntomas, dependiendo de las neuronas afectadas. No se comprende completamente qué células del sistema inmunitario y qué dianas proteicas desempeñan un papel clave en el inicio y la progresión de la esclerosis múltiple, y dicha información podría ayudar al desarrollo de nuevos tratamientos. En un reciente estudio Jelcic y colaboradores presentan un análisis de las células del sistema inmunológico en personas con esclerosis múltiple, lo que permite profundizar la comprensión de cómo las células inmunitarias pueden contribuir a esta enfermedad (DOI: 10.1016/j.cell.2018.08.011).
Un factor relacionado con el riesgo de desarrollar esclerosis múltiple es la posesión de una versión particular de una proteína llamada HLA. Las proteínas HLA permiten a las células mostrar antígenos - fragmentos de proteínas - en sus superficies. Si el receptor de un antígeno (el receptor de células T; TCR) en una célula T reconoce un antígeno presentado por una proteína HLA, la célula T se activa para desencadenar una respuesta inmunitaria contra las células que expresan el antígeno. Las variaciones en la capacidad de unión de antígenos de diferentes proteínas HLA y en la capacidad de reconocimiento de antígenos de los TCR permiten que el cuerpo responda a una amplia gama de antígenos asociados con los microorganismos causantes de enfermedades. Sin embargo, existe el peligro de que si una proteína HLA se une eficientemente a un antígeno que normalmente forma parte del cuerpo, y si se activa una célula T que reconoce el complejo antígeno HLA, se desarrolle autoinmunidad. Tal mecanismo podría subyacer al hecho de que la versión de HLA llamada HLA-DR15 es un factor de riesgo para la esclerosis múltiple, y se estima que contribuye con el 60% del riesgo genético total para desarrollar la enfermedad.
Las células T de personas con esclerosis múltiple son más propensas a dividirse in vitro que las células T de personas sanas. Esta división celular es similar a la que se produce como resultado de la activación normal de las células inmunitarias por un estímulo antigénico, pero en este caso no parece requerir la adición de tal evento a la muestra de células inmunitarias. Esto sugiere que el requisito normal para el reconocimiento de antígenos se está pasando por alto, o que estas células T reconocen un antígeno que está presente en otras células inmunitarias en la muestra de sangre. Jelcic y sus colegas investigaron más a fondo, analizando con más detalle el comportamiento de las células inmunitarias en muestras de sangre de personas con esclerosis múltiple. Demuestran convincentemente que tanto las células T como las células B de estas muestras podrían proliferar cuando se cultivan in vitro. Los autores denominan este tipo de división autoproliferación, porque ocurre espontáneamente in vitro sin la adición de un antígeno.
Los autores encontraron que la señalización a través de una proliferación de células T iniciada por TCR, y que la proliferación celular estaba asociada con la producción de IFN-γ por parte de las células T (figura 1), lo que a su vez se asocia con la esclerosis múltiple. El IFN-γ es un potente activador de una categoría de células inmunitarias llamadas macrófagos, que dañan directamente la vaina de mielina en la esclerosis múltiple.
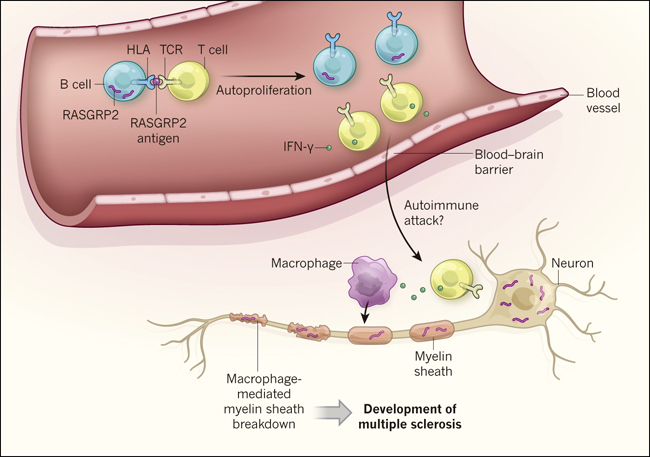
Figura 1: acción inmunocelular asociada a la esclerosis múltiple.
Jelcic y sus colegas (DOI: 10.1016/j.cell.2018.08.011) reportan que las células B del sistema inmunológico presentes en el torrente sanguíneo producen una proteína llamada RASGRP2. Estas células utilizan una proteína llamada HLA para presentar un fragmento peptídico (un antígeno) de RASGRP2 en su superficie celular. Si este antígeno es reconocido por el receptor de células T (TCR) esta interacción conduce a la proliferación ambos tipos celulares, linfocitos T y B, un fenómeno que los autores llamaron autoproliferación. Su evidencia indica que estas células T autoproliferativas pueden, por una ruta desconocida, cruzar la barrera hematoencefálica para entrar en el cerebro. El RASGRP2 también se encuentra en el tejido cerebral. Si las neuronas u otras células cerebrales expresan RASGRP2, esto podría desencadenar que las células T que se infiltran en el cerebro orquesten un ataque autoinmune produciendo mediadores inflamatorios. Por ejemplo, la producción de proteínas IFN-γ por células T activadas podría estimular a los macrófagos del sistema inmunológico, que son conocidos por atacar la estructura de la vaina de mielina que protege las fibras nerviosas y que poya la función neuronal. Esto, a su vez, podría conducir al desarrollo de la esclerosis múltiple.
Los autores sugieren que la proliferación de células B impulsa la autoproliferación de células T, porque ni las células T ni las B se dividen si las células cultivadas se exponen a un fármaco llamado ibrutinib. El ibrutinib inhibe la proteína BTK, que es esencial para la señalización río abajo del receptor de antígeno de células B que conduce a su proliferación. Curiosamente, un ensayo clínico de fase IIb (ver go.nature.com/2yhfphu) ha reportado evidencia preliminar de que el inhibidor del BTK evobrutinib podría potencialmente proporcionar beneficios para las personas con esclerosis múltiple (ver go.nature.com/2qtqby9).
Cada uno de los tratamientos para la esclerosis múltiple actualmente en uso suprime la inflamación cerebral asociada a la enfermedad, pero de diferentes maneras. Los investigadores aprovecharon esta oportunidad para probar si las interacciones entre las células B y las T son necesarias para la autoproliferación de células T, y si este fenómeno podría estar involucrado en procesos que conducen a los síntomas de la esclerosis múltiple.
Los autores analizaron muestras de sangre de personas con la enfermedad que recibían diferentes tratamientos antiinflamatorios y compararon estos resultados con controles de personas con la enfermedad que no recibían tratamiento. Para aquellos que reciben un anticuerpo llamado natalizumab, que causa un aumento en el número de células T y células B inmaduras en la sangre, el análisis in vitro mostró que la autoproliferación de células B y células T aumentó en comparación con los controles. Las muestras de aquellos que recibieron un anticuerpo llamado rituximab, que elimina linfocitos B sanguíneos, tuvieron una proliferación de células T muy reducida en comparación con los controles.
Este análisis del efecto de los tratamientos antiinflamatorios que afectan a las células T o B aporta pruebas coherentes con el modelo de los autores de que las interacciones clínicamente relevantes entre ambos tipos de linfocitos se producen en la esclerosis múltiple. Durante muchos años, se pensó generalmente que las células B no tenían un rol en la esclerosis múltiple, debido a los resultados de estudios en animales. Esta opinión cambió cuando se observaron beneficios sorprendentes en ensayos clínicos de la reducción de las células B para el tratamiento de la esclerosis múltiple.
Jelcic y sus colegas necesitaban responder a la pregunta de si las células T autoproliferativas contribuyen al desarrollo de la esclerosis múltiple. Para abordar este difícil problema, los autores analizaron los descendientes celulares de células T individuales que proliferan a partir de la sangre de personas con esclerosis múltiple. Observaron las fracciones variables de los TCRs presentes en las células porque estas regiones proporcionan un patrón único, similar a un código de barras, que puede identificar cualquier célula T y sus descendientes genéticamente idénticos - que forman un linaje celular llamado clon.
Mediante experimentos rigurosos y desafiantes, usando material de dos personas que tenían esclerosis múltiple, los autores analizaron las células T encontradas en el tejido cerebral tomadas en la biopsia o en la autopsia y las compararon con las células T de las muestras de sangre de la misma persona tomadas antes de que se obtuvieran las muestras de tejido cerebral. Los autores encontraron que las células T de muestras de sangre que se sometieron a autoproliferación in vitro pertenecían a un linaje celular idéntico que coincidía con las células T encontradas en las muestras de tejido cerebral tomadas de la misma persona.
Este hallazgo sugiere fuertemente que algunas células que proliferan en la sangre de las personas con esclerosis múltiple podrían entrar en su cerebro. Una vez allí, tales células T podrían liberar moléculas de señalización inmunológica como el IFN-γ que estimula los macrófagos, los que podrían iniciar una lesión tisular inflamatoria. Las células inmunitarias siempre están presentes en el líquido cefalorraquídeo que recubre el cerebro y la médula espinal, y las células T productoras de IFN-γ y las células T proliferantes han sido previamente identificadas en el líquido cefalorraquídeo de individuos con esclerosis múltiple. Por lo tanto, los hallazgos resaltan la importancia de las observaciones previas y brindan apoyo adicional a los modelos establecidos de cómo progresa esta enfermedad.
Queda un último dilema: ¿cuáles son las dianas antigénicas de estas células T? Esta es una pregunta clave porque no se han identificado definitivamente los autoantígenos relevantes que provocan la esclerosis múltiple. Para intentar responder a esta pregunta, los autores analizaron una población de células clónicas cultivadas in vitro, derivadas de una célula T y sus descendientes que estaban presentes en la sangre y en el cerebro post-mortem de una persona con esclerosis múltiple. Jelic y sus colegas utilizaron un enfoque innovador que se basó en la evaluación computacional de los datos obtenidos mediante métodos estándar para estimular las células T. Los autores evaluaron un número casi inimaginablemente grande de péptidos estructuralmente similares pero no idénticos en cuanto a su capacidad para actuar como antígeno que generaría una respuesta de esta población de células T. Descubrieron un antígeno de la proteína RASGRP2 como uno que probablemente estimula al TCR de esta población de células T. El RASGRP2 no se había vinculado anteriormente a procesos relacionados con la esclerosis múltiple. Los autores demostraron que RASGRP2 se expresa tanto en las células B que provocan la proliferación de células T como en el tejido cerebral.
El estudio de Jelcic y sus colegas proporciona un modelo de cómo las interacciones entre las células B y las células T fuera del cerebro podrían generar linfocitos T que contribuyen a la enfermedad y que luego entran en el cerebro. Su descubrimiento de un antígeno asociado con la esclerosis múltiple podría, si se identifican otros antígenos similares a futuro, revelar cómo se produce la autoinmunidad y, quizás, cómo se podría remediar.
Fuente bibliográfica
Immune-cell crosstalk in multiple sclerosis
Richard M. Ransohoff
Department of Cell Biology, Harvard Medical School, Boston.
doi: 10.1038/d41586-018-07063-z