La vía alérgica en el dolor abdominal
Recientes hallazgos basados en animales sugieren que un mecanismo inmunológico periférico puede subyacer a los síntomas asociados al dolor abdominal en pacientes con síndrome del intestino irritable.
Los síntomas gastrointestinales son frecuentes en niños y adultos, que incluyen dolor abdominal después de las comidas. Millones de personas tienen sintomatología crónica definida como el dolor gastrointestinal funcional o síndrome del intestino irritable (SII) sin causa identificable. Esta situación es frustrante paro todos, ya que hay pocos tratamientos efectivos y los que están, no brindan un alivio satisfactorio a la mayoría de los pacientes. Además, los médicos suelen tener la impresión de que la condición es mental.
Una teoría predominante del SII se relaciona con el eje intestino-cerebro. Esta sostiene que los síntomas pueden ser causados por un sistema nervioso en el tracto gastrointestinal demasiado sensible y la forma en que se procesan sus señales en el cerebro. De hecho, los nervios intestinales de tales pacientes son hipersensibles a una variedad de estímulos y, por lo tanto, las funciones diarias, como el estiramiento gastrointestinal y la motilidad alimentaria, resultan más dolorosas que individuos no afectados. Durante períodos de estrés emocional o físico (por ejemplo, ansiedad o infección), los síntomas se agravan debido a la estrecha relación entre el cerebro y el intestino.
Se plantea la idea de que una interacción entre el sistema inmunológico y el sistema nervioso entérico provocaría los síntomas gastrointestinales idiopáticos. La gastroenteritis infecciosa es un factor de riesgo para el SII; muchas infecciones entéricas conducen a su aparición, y los pacientes con SII a menudo señalan que su sintomatología comienza con una infección gastrointestinal. Además, los aumentos en el número de mastocitos y en la liberación de mediadores, incluidas sustancias neurotrópicas, podrían implicarse en la hipersensibilidad visceral.
Los mastocitos son glóbulos blancos que residen en varios tejidos cercanos a las interfaces de las mucosas, especialmente los que están próximos a los vasos sanguíneos y a las fibras nerviosas. Se les conoce clásicamente por su papel en las reacciones alérgicas; albergan receptores de alta afinidad por IgE y suelen liberar rápidamente mediadores, como la histamina, después de la exposición a alérgenos. Un estudio reciente de Javier Aguilera-Lizarraga y colegas sugiere que un mecanismo inmunológico periférico que involucra a mastocitos locales estimulados por la IgE local inducida por los alimentos puede subyacer a los síntomas asociados con el SII y al dolor abdominal funcional; estos hallazgos avalan nuevas estrategias terapéuticas que puedan hacer frente a los mastocitos y las alergias.
Ellos estudiaron si la tolerancia normal a los antígenos orales (alimento) en ratones se perdería si los animales fueran infectados simultáneamente con una bacteria intestinal experimental (Citrobacter rodentium) y alimentados con antígenos de clara de huevo (ovoalbúmina). Una vez que la infección intestinal desapareció, los ratones ingirieron de nuevo la ovoalbúmina; esta vez, presentaron dolor abdominal, evaluado por las contracciones de los músculos del estómago. Estos ratones también tenían diarrea y un tiempo de tránsito intestinal reducido. Por el contrario, los que no recibieron ovoalbúmina durante la infección intestinal no presentaron efectos similares ni otras anomalías. Además, en aquellos inoculados con bacterias y ovoalbúmina, los anticuerpos IgE específicos de la proteína estaban presentes en el colon, el sitio colonizado por C. rodentium, pero no en el intestino delgado ni en el suero. En estos animales, la ingestión de agentes que interferían con la alergia como anti-IgE, estabilizadores de mastocitos y antagonistas del receptor de histamina H1, atenuaba las respuestas patológicas y sintomáticas. Además, los que fueron modificados genéticamente para ser deficientes en mastocitos o en el receptor de histamina H1 se encontraban protegidos en un grado similar a los controles. La estimulación de los nervios esplácnicos del colon, que transmiten señales de dolor visceral a la médula espinal, indujo una mayor excitabilidad neuronal en ratones alérgicos versus los controles, efecto que podía bloquearse con antihistamínicos. Estos hallazgos indican que una infección bacteriana gastrointestinal puede romper la tolerancia oral a un antígeno de la dieta y dar como resultado una respuesta inmune adaptativa hacia ese antígeno, lo que a su vez conduce a una mayor permeabilidad intestinal y a una señalización anormal de dolor cuando se produce la reexposición al antígeno (figura 1).
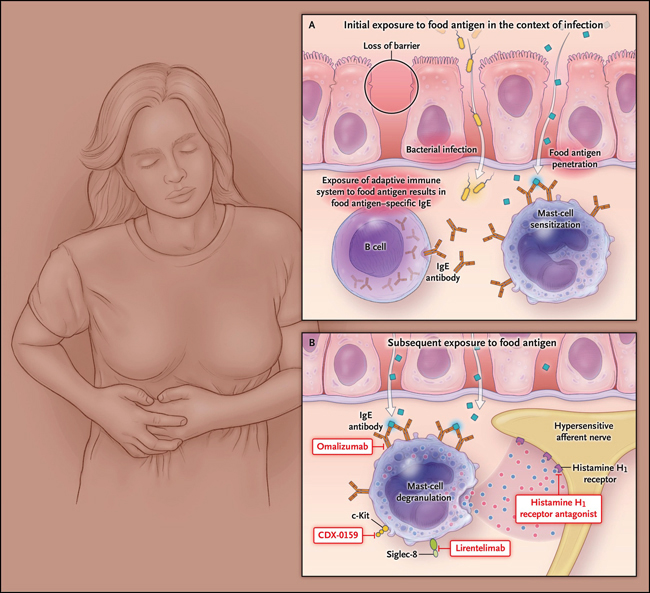
Figura 1: respuesta inmune alérgica y síntomas gastrointestinales inducidos por alimentos.
Un reciente estudio apoya la teoría de que un mecanismo inmunológico periférico que involucra a los mastocitos estimulados por la IgE local e inducida por alimentos puede ser la base de los síntomas asociados con el síndrome del intestino irritable y el dolor abdominal funcional, lo que lleva a considerar nuevas estrategias terapéuticas. En personas con predisposición genética al síndrome del intestino irritable, la infección bacteriana desencadena una pérdida de la función de barrera en el colon. Posteriormente, los alérgenos alimentarios penetran en la mucosa y conducen a la sensibilización por IgE y a la carga de los mastocitos con IgE unida a la superficie (panel A). Después de la reexposición a alérgenos, los mastocitos locales que portan IgE específica se desgranulan, lo que da como resultado la liberación de mediadores neurotrópicos, incluida la histamina. La exposición a estos mediadores hace que los nervios aferentes sean hipersensibles y la hipersensibilidad puede persistir incluso en ausencia del antígeno desencadenante. Los objetivos de una posible intervención terapéutica incluyen la IgE (dirigida por omalizumab), inhibición de los mastocitos (con el uso de lirentelimab, que se une a Siglec-8, un receptor expresado por los mastocitos), el control de los mastocitos (a través de anticuerpos anti-c- Kit) y receptores antihistamínicos.
¿Estos resultados se pueden aplicar a los pacientes? Los autores exploraron si 12 personas con SII y 8 controles tendrían respuestas de los mastocitos desencadenadas por los alimentos. Los resultados no mostraron evidencia de IgE sistémica contra alimentos comunes, resultados consistentes con los observados en ratones. Sin embargo, cuando se inyectaron alérgenos comunes en la mucosa rectal, cada paciente con SII tuvo una reacción localizada a al menos uno de los antígenos; 2 de los 8 participantes tuvieron una reacción a un solo alérgeno.
¿Debería este estudio cambiar nuestra visión de los síntomas gastrointestinales funcionales y el SII? Posiblemente, pero aún hay más por saber, en parte porque la traducción de los hallazgos en ratones se basa en una prueba de investigación no convencional (inyección de antígenos en la mucosa rectal) en un número muy pequeño de participantes humanos. También queda por determinar cuáles de los mediadores de mastocitos, si los hay, estarían involucrados en la enfermedad humana. El examen de mastocitos en muestras de biopsia gastrointestinal humana no se realiza de forma rutinaria y puede requerir la medición de la proximidad de los mastocitos a las terminaciones nerviosas, una tarea desafiante. Los datos de otros ensayos realizados proporcionaron evidencia preliminar de que las dosis altas y prolongadas de un antagonista del receptor de histamina H1 reducen la hipersensibilidad visceral, los síntomas y el dolor abdominal en el SII. Además del esquema antihistamínico, existen y surgen terapias dirigidas que bloquean las vías alérgicas, pudiendo tener valor en el tratamiento de los síntomas funcionales del SII y de otras enfermedades (figura 1).
Es evidente que la alergia a los alimentos no es una patología que involucre solo reacciones sistémicas mediadas por IgE. Más bien, existe un espectro de respuestas alérgicas inducidas por alimentos, con anafilaxia sistémica mediada por IgE en un extremo y respuestas alérgicas específicas del tejido gastrointestinal en el otro extremo. En el centro se encuentran las enfermedades en las que segmentos específicos del tracto gastrointestinal son sitios de respuestas alérgicas locales inducidas por alimentos, como las de mastocitos específicas del colon descritas aquí, y las respuestas eosinofílicas del esófago en la esofagitis eosinofílica. Una diferencia fundamental entre las respuestas alérgicas definidas por el equipo de Aguilera-Lizarraga y la alergia alimentaria clásica es que los anticuerpos IgE específicos de ovoalbúmina identificados por eran detectables solo en el tejido colónico, indicando una respuesta inmune local más que sistémica contra los antígenos de la dieta. La naturaleza específica probablemente implique una interacción de factores genéticos y ambientales, como se ha descubierto en la esofagitis eosinofílica, cuyo riesgo está asociado a variantes genéticas en una vía de la mucosa esofágica. En resumen, aunque queda mucho por dilucidar, estos datos apoyan la hipótesis de que algunas dolencias gastrointestinales, como el SII y dolor abdominal funcional, pueden ser trastornos alérgicos inducidos por alimentos.
Fuente bibliográfica
An Allergic Basis for Abdominal Pain
Marc E. Rothenberg, M.D., Ph.D.
Division of Allergy and Immunology, Department of Pediatrics, Cincinnati Children’s Hospital Medical Center, University of Cincinnati College of Medicine, Cincinnati.
N Engl J Med 2021; 384: 2156-2158