Vacunas anticancerígenas personalizadas
Un objetivo del tratamiento del cáncer es la erradicación de células tumorales, mientras que se mantiene la estabilidad de las células sanas. Los enfoques convencionales como la quimioterapia o el tratamiento con fármacos específicos muestran tal selectividad pero a menudo son tóxicos. El sistema inmunológico puede dirigirse específicamente a las células tumorales, pero estas respuestas de defensa con frecuencia son suprimidas dentro de un tumor o en sus alrededores. Aunque los nuevos enfoques de la inmunoterapia pueden ayudar a superar esta supresión al apuntar a una de las vías comprometidas con la inmunidad celular (la vía del receptor PD-1), estos tratamientos pueden asociarse con importantes efectos secundarios. Investigaciones realizadas en modelos de ratón y estudios clínicos han permitido aumentar la capacidad de la respuesta inmune hacia los tumores mediante estrategias de vacunación que apuntan a las proteínas mutantes presentes en las células tumorales, lo que implica un gran avance y un esperanzador descubrimiento.
Detección de neoantígenos
La estrategia de vacunación para desencadenar una respuesta antitumoral específica por parte de las células T puede consistir en la introducción en el cuerpo de fragmentos de péptidos conocidos como antígenos, que se presentan al sistema inmune cuando se encuentra unido por proteínas del complejo mayor de histocompatibilidad (MHC). Para tener éxito, las vacunas contra el cáncer deben satisfacer varios criterios clave. Uno de ellos es la incorporación de de antígenos tumorales específicos que pueden inducir respuestas inmunitarias potentes de las células T. Antígenos que surgen en un tumor por una mutación y que normalmente no están presentes en las personas sanas (neoantigenos) entran en esta categoría.
Otro aspecto esencial es la selección del enfoque vacunal adecuado. Las vacunas deben entregar efectivamente los productos constituyentes, como por ejemplo, materiales sintéticos de larga duración como péptidos, ADN y ARN, que proporcionan una fuente concentrada de antígenos y que pueden utilizarse por el cuerpo para generar antígenos. Las vacunas también deben incluir un componente conocido como adyuvante, el que proporciona un estímulo inmunológico general que permite una mayor respuesta contra el tumor. Otra parte importante de la estrategia de vacunación es contrarrestar la supresión de las células T en el microambiente del cáncer en pacientes que tienen tumores residuales o recurrentes después de la terapia.
En dos recientes publicaciones Ott y sus colegas (doi: 10.1038/nature22991) y Sahin y colaboradores (doi: 10.1038/nature23003) reportaron los resultados de ensayos clínicos fase I que evaluaron enfoques basados en vacunas para tratar personas con cáncer de piel. Los investigadores analizaron pacientes que tenían una etapa avanzada de un tipo común de cáncer de piel llamado melanoma. Muchos melanomas ocurren por la exposición a la luz solar, y están asociados con un gran número de mutaciones aleatorias en el ADN en células conocidas como melanocitos. Las mutaciones que están causalmente involucradas en el crecimiento de un tumor son infrecuentes -la mayoría de las veces las mutaciones no promueven el crecimiento tumoral. Pero estas mutaciones podrían generar secuencias de proteínas anormales que no están presentes en otras partes del cuerpo y, por lo tanto, son objetivos potenciales para obtener o reforzar una respuesta inmune específica contra el tumor.
El grupo de Ott y colaboradores vacunó a seis personas que previamente se habían sometido a cirugía para extirpar un tumor. Para diseñar vacunas personalizadas, los autores secuenciaron el ADN de las células tumorales y de células sanas de cada persona para identificar mutaciones específicas y determinar neoantígenos asociados. Luego usaron un algoritmo para predecir cuál de los neoantigenos se uniría firmemente a las proteínas MHC. Cada participante fue vacunado con vacunas péptidos sintéticos largos que representen hasta 20 neoantigenos específicos de cada paciente. Dichos péptidos se presentan a las células T por medio de la acción de las células presentadoras de antígenos del sistema inmunológico.
Por su parte, el grupo de Sahin y sus colegas utilizó un tipo similar de sistema personalizado para identificar neoantigenos que se unen con alta afinidad a las proteínas MHC. En su estudio, 13 personas que estaban experimentando tratamiento para el melanoma, los autores seleccionaron hasta diez mutaciones por persona para crear una vacuna basada en ARN que fue adaptada para el tumor de cada individuo. Los autores habían demostrado previamente que tales moléculas de ARN pueden ser absorbidas por las células presentadoras de antígenos.
Si un antígeno unido a MHC es reconocido por un receptor de la célula T (localizado en la superficie celular), ésta puede montar una respuesta contra cualquier célula que contenga tal antígeno. Existen dos tipos de proteínas MHC, y estas presentan antígenos a diferentes tipos de células T. Las proteínas MHC clase I presentan antígenos a linfocitos T citotóxicos CD8+, los cuales expresan la proteína CD8 en su membrana plasmática. Estas células T pueden montar un ataque que mata directamente las células que expresan el antígeno especificado. Las células que no son parte del sistema inmunitario, incluyendo las tumorales, por lo general también tienen MHC clase I en sus superficies.
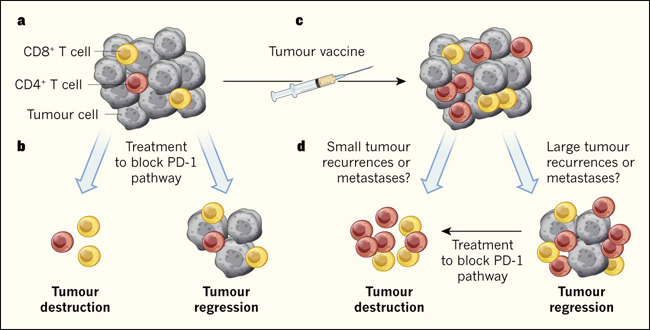
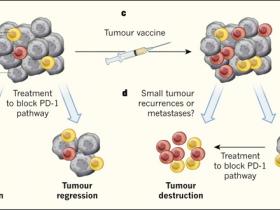
Figura 1. Manipulación de la respuesta inmunológica frente a los tumores.
Contrariamente las proteínas del MHC clase II se encuentran solo en células del sistema inmunológico. Presentan antígenos a las células T que expresan la proteína CD4, conocidos como linfocitos T helper CD4+. Los antígenos tumorales pueden ser exhibidos a este tipo celular mediante células presentadoras de antígenos que incorporan material celular de restos celulares o células tumorales moribundas. El reconocimiento directo del tumor por parte de linfocitos CD4+ ha sido documentado previamente y estas células también están asociadas con la destrucción directa de las células tumorales Los linfocitos T helper CD4+ tienen un papel adicional en optimizar la función de su contraparte celular los linfocitos T citotóxicos CD8+ y en ayudar a la generación de células T CD8+ con un capacidad de memoria que permite una mayor y más rápida respuesta en un encuentro posterior con un antígeno específico.
Las vacunas desarrolladas generaron respuestas de linfocitos CD4+ y CD8+, que probablemente dieron lugar a la activación de células T CD4+, a células presentadoras de antígenos y células T CD8+, así como a interacciones necesarias entre estas células para permitir una acción y memoria linfocítica. Los hallazgos de ambos estudios revelaron que las vacunas aumentaron el número de células T que participan en la respuesta inmunitaria, fenómeno previamente observado contra ciertos neoantigenos, y generaron respuestas de células T contra otros neoantigenos que no se habían observado antes.
Los dos estudios confirman el potencial de este tipo de enfoques, y las mejoras en la predicción neoantigénica probablemente permitirán una identificación aún más eficaz y precisa de neoantígenos para su uso en próximas vacunas terapéuticas. Aunque el número de personas que fueron tratados en estos estudios es pequeño, ambas investigaciones obtuvieron beneficios potenciales. Por ejemplo, después de la vacunación, se observaron menos episodios de recurrencia o migración tumoral a otras partes del cuerpo (metástasis). Sahin y sus colegas notaron que los participantes mostraron una tasa significativamente menor de metástasis después de la vacunación. En los casos en que los tumores persistieron o producían un rebrote, esto podría combatirse eficazmente mediante el tratamiento dirigido a la vía del receptor PD-1 (Figura 1). Por lo tanto, se hacen necesarios estudios controlados y randomizados de fase II que incluyan más participantes para confirmar y establecer la eficacia de estas vacunas en pacientes con cualquier tipo de cáncer que contengan mutaciones suficientes para proporcionar los neoantígenos necesarios para implementar este tipo de terapia.
Fuente bibliográfica
Cancer: Precision T-cell therapy targets tumours
Cornelis J. M. Melief
Department of Immunohematology and Blood Transfusion, Leiden University Medical Center, Leiden.
doi:10.1038/nature23093