Mutaciones impulsan la hematopoyesis clonal tras quimioterapia
Particularmente las alteraciones en el gen PPM1D otorgan a las células sanguíneas sometidas a tratamiento citotóxico una ventaja selectiva que favorece la posterior aparición de leucemia.
Uno de los riesgos más graves de la quimioterapia citotóxica contra el cáncer es el desarrollo de neoplasias malignas hematopoyéticas secundarias algunos años después. En teoría, este tratamiento y la radiación pueden infligir directamente daño al ADN, el que al ser reparado de manera inapropiada, produce subsiguientes mutaciones que conducen al cáncer. También es posible que las terapias puedan ejercer presiones selectivas sobre las células madre hematopoyéticas, de manera que ciertas poblaciones mutantes (conocidas como clones) tengan una ventaja selectiva en condiciones citotóxicas. Si los clones mutantes sobreviven más tiempo, pueden acumular más mutaciones. Esta podría ser la razón por la cual la expansión de los clones mutantes, conocida como hematopoyesis clonal (HC), está asociada con un mayor riesgo de desarrollar tumores hematológicos malignos.
Dado que las mutaciones en la proteína fosfatasa dependiente de magnesio/manganeso 1 D (PPM1D) -una reguladora de la respuesta al daño del ADN- se han vinculado con la HC en pacientes con exposición previa a tratamiento citotóxico, se realizó una investigación con leucemia mieloide aguda relacionada con la terapia (t-AML, por sus siglas en inglés) y el síndrome mielodisplásico relacionado con tratamiento, complicaciones que surgen en algunos individuos años después de la quimioterapia contra tumores sólidos o neoplasias malignas hematológicas no mieloides.
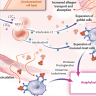
Los resultados de la investigación mostraron que las mutaciones en PPM1D estaban presentes en una quinta parte de los pacientes con t-AML o síndrome mielodisplásico y se encontraban fuertemente correlacionadas con la exposición al cisplatino. En ensayos realizados en líneas se observó que las mutaciones hiperactivas en PPM1D se expanden para superar a las células normales después de la exposición a agentes citotóxicos que dañan el ADN, incluido el cisplatino, y este efecto fue mediado predominantemente por una mayor resistencia a la apoptosis. Además, las células hematopoyéticas mutantes Ppm1d heterocigóticas superaron en competencia a sus contrapartes de tipo silvestre en un modelo animal después de la exposición al cisplatino y la doxorrubicina, pero no durante la recuperación del trasplante de médula ósea.
En suma, estos hallazgos establecen la relevancia clínica de las mutaciones en PPM1D en la hematopoyesis clonal y la importancia de estudiar las interacciones mutación-tratamiento.
Temas Relacionados