Tratando el exceso hierro
La sobrecarga de hierro es una condición que afecta a millones de personas en todo el mundo. El exceso de hierro en el cuerpo es tóxico, y los depósitos pueden causar daños en hígado, corazón y otros órganos. Los tratamientos actuales, dicen los especialistas, no son ideales y tienen efectos secundarios significativos. El hierro en el cuerpo está regulado por una hormona llamada hepcidina, y su carencia genera altas concentraciones férricas, como se ha observado en ciertos trastornos genéticos, como la hemocromatosis hereditaria y la anemia de Cooley. Este péptido se sintetiza en el hígado y ejerce su función a través de la degradación de la proteína ferroportina, situada en el epitelio intestinal y en la membrana de los macrófagos, siendo su principal función la de transportar el hierro desde la célula intestinal al plasma y desde el macrófago al eritrón.
Hepcidina y ferroportina
La hemocromatosis genética es una enfermedad causada por la acumulación excesiva de hierro resultante de la producción inadecuada de hepcidina, la principal hormona reguladora de hierro. Recientemente, Gloria C. Preza y colaboradores (J Clin Invest. 2011 Dec 1; 121(12):4880-8) desarrollaron una hepcidina oral biológicamente activa que ofrece un novedoso enfoque experimentalmente para el tratamiento de la hemocromatosis y otras condiciones caracterizadas por la acumulación anormal de hierro.
La fisiología del hierro en los mamíferos es compleja, pero el conocimiento de dos proteínas - la hepcidina y ferroportina - da una idea sobre la mayoría de los trastornos relacionados (figura 1). La ferroportina es un exportador transmembrana de hierro que lo transfiere fuera de las células. Esta proteína es importante en el epitelio intestinal, ya que permite que el hierro de la dieta sea captado por las células de absorción para que ingrese a la circulación, y que los macrófagos reciclen el hierro utilizado por los glóbulos rojos. La hepcidina, un pequeño péptido producido por el hígado, controla la actividad de la ferroportina al unirse a ella y dirigirla a la proteína para su destrucción en el lisosoma. Los niveles de hepcidina fluctúan en respuesta a las necesidades de hierro corporal. En términos simples, más hepcidina provoca una menor absorción de hierro, y menos hepcidina mayor absorción (figura 1).
La mayoría de los trastornos del balance de hierro se pueden atribuir a la producción aberrante de hepcidina. La anemia por deficiencia de hierro refractaria al hierro (IRIDA, por sus siglas en inglés) es una condición genética que se caracteriza por una producción elevada de hepcidina, limitando la absorción y utilización del hierro. La anemia, una enfermedad crónica y multifactorial, se explica principalmente por la gran producción de hepcidina en respuesta a las citoquinas inflamatorias. Por el contrario, la hemocromatosis es el resultado de mutaciones en genes que normalmente inducen la expresión de hepcidina, y su gravedad se correlaciona inversamente con los niveles de hepcidina. Pruebas experimentales en ratones han demostrado que un aumento artificial de la expresión de hepcidina impide la hemochromatosis. En la talasemia y otras anemias que se complican por la sobrecarga secundaria de hierro, la disminución de hepcidina lleva a una mayor absorción de hierro, lo que agrava la sobrecarga de hierro en terapias de transfusión a largo plazo. Sorprendentemente, el tratamiento genético de los ratones talasémicos con hepcidina no sólo mejoró la sobrecarga de hierro, sino también la eritropoyesis. Por lo tanto, la manipulación de los niveles de hepcidina podría ser útil en una variedad de trastornos. Desgraciadamente, esta terapia en sí misma no es factible en humanos, debido a que el péptido nativo es técnicamente difícil de producir en cantidades suficientes.
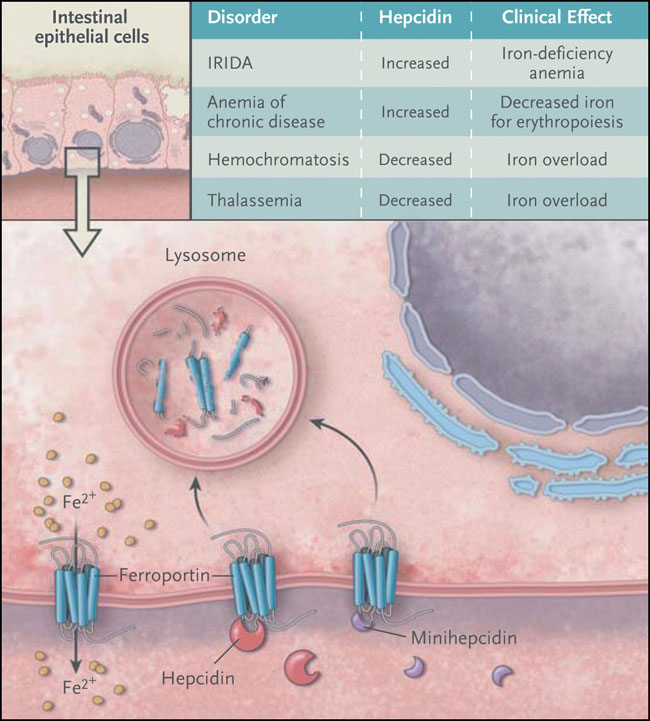
La ferroportina, el exportador transmembrana de hierro más importante, actúa en las células epiteliales intestinales, en macrófagos recicladores de hierro y en otras células que transfieren el hierro a la circulación. Su actividad está controlada por la hepcidina, una hormona peptídica que se une a un bucle extracelular de ferroportina para activar su internalización y degradación lisosomal. Este estudio ha desarrollado minihepcidinas que imitan la actividad del péptido hepcidina natal. La mayor actividad de la hepcidina conduce a la deficiencia de hierro y de eritropoyesis, como se ha observado en la anemia ferropénica (IRIDA) y en la anemia de enfermedad crónica. La menor actividad de la hepcidina mejora la absorción intestinal de hierro y la sobrecarga, aspectos asociados con la hemocromatosis y la talasemia.
G. Preza y colegas llevaron a cabo estudios estructurales de la hepcidina y ferroportina para determinar qué partes de cada molécula eran importantes para su interacción molecular. Se concentraron en los primeros nueve aminoácidos del péptido hepcidina humano, fragmento capaz de unirse a la ferroportina y provocar su degradación. Usaron un truco bioquímico para producir el péptido sintético llamado minihepcidina al vincular los D-estereoisómeros de cada aminoácido en orden inverso para crear un péptido similar en estructura a la parte funcional de la hepcidina nativa, pero mucho más resistente a la proteolisis in vivo. Asimismo, modificaron esta molécula para aumentar su solubilidad, reducir la inmunogenicidad, ser absorbible en forma oral y disminuir la depuración renal.
Varias de las minihepcidinas más potentes que fueron probadas en ratones mostraron una reducción de la concentración de hierro sérico y evitaron su acumulación en el hígado, indicando que fueron efectivas. Este es un buen augurio para futuros estudios en humanos, debido a que las interacciones entre la hepcidina y ferroportina en ratones y personas son muy similares.
La terapia agonista de la hepcidina, obviamente, sería ventajosa en el tratamiento de la hemocromatosis. Sin embargo, el manejo estándar que se ha utilizado por más de 60 años – la flebotomía - es seguro y barato. Aunque la hemocromatosis es una patología frecuente, los pacientes podrían preferir una alternativa a la flebotomía, lo que podría ser difícil de cumplir, principalmente por el desarrollo de un nuevo medicamento. Sin embargo, existe una urgente necesidad de reducir la absorción de hierro en pacientes con síndromes de talasemia o sobrecarga de hierro secundaria asociada a otras anemias congénitas (anemia sideroblástica y anemia diseritropoyética congénita), ya que estas personas por lo general no pueden someterse a flebotomía debido a su condición subyacente - una mercado mucho menor que para el tratamiento de la hemocromatosis. Teóricamente, es posible que la terapia agonista con hepcidina pudiera ir más allá de bloquear la absorción de hierro y potenciar la excreción de hierro.
Esto podría ser posible mediante aspectos bioquímicos relacionados con la búsqueda de agonistas de la hepcidina para desarrollar antagonistas de la hepcidina - es decir, moléculas que protegen a la ferroportina de la destrucción inducida por hepcidina. Los antagonistas de la hepcidina podrían aliviar la anemia en pacientes con IRIDA y anemia de enfermedad crónica. Es posible que los antagonistas de la hepcidina puedan tener un uso aún más amplio mediante la aceleración de reposición de hierro por vía oral en pacientes con anemia ferropénica. Tanto la anemia por enfermedad crónica como la anemia por deficiencia de hierro ofrecen grandes campos para el desarrollo de fármacos.
Fuente bibliográfica
Closing the Iron Gate
Nancy C. Andrews, M.D., Ph.D.
Duke University School of Medicine, Durham, NC.
N Engl J Med 2012; 366:376-377