Armonía inflamatoria en el asma
Los cisteinil leucotrienos (CysLT) son potentes mediadores profilácticos en los pacientes asmáticos. Sin embargo, la inhibición del receptor 1 de los CysLT no es un tratamiento sistemáticamente eficaz, lo que sugiere la existencia de mecanismos de regulación adicionales. Recientemente se han descubierto otros mediadores lipídicos que contienen cisteinil derivados del ácido docosahexaenoico, como los conjugados de maresina en la regeneración de tejidos (MCTR). Por lo tanto, su producción y sus acciones en el pulmón son de considerable interés. La administración exógena de MCTR pulmonares que bloquean la contracción de las vías respiratorias inducida por leucotrienos D4 en humanos y que promueven la resolución de las respuestas alérgicas en modelos murinos revelan importantes los mecanismos de resolución de la respuesta inflamatoria pulmonar, como el caso de pacientes asmáticos.
Mediadores químicos y resolución
La inflamación y su oportuna resolución representan una respuesta fisiológica vital ante la infección, lesión y la "provocación estéril" por estímulos endógenos. Existe una creciente apreciación de que la iniciación, progresión y resolución de la respuesta inflamatoria y el retorno del tejido a su estado original son el resultado de procesos dinámicos. Los mediadores y mecanismos que impulsan la inflamación aguda están bien definidos y son blanco de numerosos antiinflamatorios. Pero la resolución efectiva de la respuesta no sólo se basa en la disipación de las señales que la impulsan, sino también en la activación de tipos celulares específicos y en la generación de factores solubles, incluyendo citoquinas, péptidos y mediadores lipídicos. Cuando la inflamación no se resuelve, la inflamación de bajo nivel, insidiosa y continua da lugar a numerosos estados patológicos.
Los instigadores químicos de la inflamación, incluyendo prostaglandinas y leucotrienos, aumentan la permeabilidad vascular y el reclutamiento de subconjuntos de leucocitos. A medida que evoluciona la respuesta inflamatoria, un cambio en la biosíntesis de los mediadores lipídicos da lugar a la generación de agentes que limitan el tráfico y la acumulación ulteriores de leucocitos al modular la expresión de moléculas de adhesión de las células endoteliales, promover la apoptosis de los leucocitos en el foco inflamatorio y efectuar su posterior eferocitosis (es decir, la eliminación de las células moribundas o muertas por los macrófagos). La remoción de estos componentes y los desechos asociados es un proceso clave en la resolución de la inflamación, estimulando la regeneración y la reparación. Los lípidos endógenos que promueven esas respuestas se denominan "mediadores de proresolución especializados", o SPM, e incluyen lipoxinas derivadas de los eicosanoides y resolvinas, protectinas y maresinas derivadas de los omega-3. Por lo general, estos agentes actúan como agonistas de distintos receptores expresados en las células inmunitarias y en diversos tipos de células del parénquima y del estroma. Es importante señalar que la generación de SPM se ha demostrado en la inflamación autolimitada en los humanos, coincidiendo con el inicio de la resolución. Además, la adición de un cóctel exógeno de SPM en el pico de la inflamación inducida experimentalmente en humanos, aceleró su resolución. En varios modelos de resolución de la inflamación impulsada por agentes patógenos, los SPM se han asociado con una mejora de la defensa del huésped. Esas respuestas modificadoras de la enfermedad son especialmente dignas de mención, dada la supresión inmunológica que puede estar asociada a los medicamentos antiinflamatorios convencionales.
Varios receptores de alta afinidad para los SPM son también blanco de los mediadores proinflamatorios, lo que pone de relieve el equilibrio crítico entre la generación de señales proinflamatorias y los SPM. La distorsión de este equilibrio (que implica niveles suprimidos de SPM) ha sido implicada en varias enfermedades, incluyendo la aterosclerosis, la enfermedad renal crónica y asma severo. Por ejemplo, se han detectado niveles más bajos de lipoxinas en el líquido de lavado broncoalveolar de personas con asma grave en comparación a personas sanas y con asma no grave. Se han generado miméticos sintéticos de los SPM por varios grupos de investigación y se ha demostrado su eficacia en modelos de inflamación aguda y crónica, apoyando el valor de un paradigma terapéutico centrado en la resolución y fibrosis inapropiadas.
Toda la familia de las maresinas (mediadores derivados de los macrófagos para la resolución de la respuesta inflamatoria) se genera a partir del ácido docosahexaenoico, las acciones concertadas de la 12-lipoxigenasa, y las subsiguientes reacciones con la glutatión S-transferasa (ya sea glutatión S-transferasa 4 o leucotrieno C4 sintasa, que también se conoce como glutatión S-transferasa 2). Las pruebas apuntan a un papel de las maresinas conjugadas con sulfuro en la reparación y regeneración críticas para la restauración de la homeostasis en el tejido inflamado y para mejorar las respuestas del huésped a la infección. Estos mediadores químicos y su actividad biológica se han conservado a lo largo de la evolución: los conjugados de maresina en la regeneración de tejidos (MCTR) median la regeneración de tejidos en planaria (gusanos planos con una extraordinaria respuesta regenerativa a las lesiones quirúrgicas) y pueden atenuar el retraso en la regeneración tisular inducido por la infección. La adición de MCTR en modelos de lesión por reperfusión es protectora del tejido, y se han detectado MCTR en células humanas.
El asma es una enfermedad común de inflamación pulmonar crónica. En las personas que la padecen, el ácido araquidónico se convierte en cisteinil leucotrienos por medio de la 5-lipoxigenasa y la leucotrieno C4 sintasa, aumentando así la permeabilidad vascular y la contracción del músculo liso (figura 1). Las respuestas a los cisteinil leucotrienos en el asma se dirigen farmacológicamente a través del antagonismo de sus receptores (como en el caso del fármaco montelukast) o a través de la inhibición de la 5-lipoxigenasa (en el caso del fármaco zileutón), pero existe una marcada heterogeneidad en la respuesta al bloqueo farmacológico. Esta heterogeneidad pone de relieve al MCTR1, MCTR2 y MCTR3, miembros de la familia de los MCTR que son antagonistas funcionales de la permeabilidad vascular inducida por leucotrienos. Estos conjugados de maresina interrumpen la unión del leucotrieno D4 a los receptores recombinantes, y las respuestas a los MCTR son parcialmente bloqueadas por un antagonista de los receptores de cisteinil leucotrieno. Dado el papel bien establecido de los cisteinil leucotrienos en el asma, Bruce Levy y colaboradores investigaron la expresión de los MCTR en el pulmón humano en un esfuerzo por determinar si impulsan la reconciliación homeostática en la enfermedad inflamatoria (J Allergy Clin Immunol. 2020 Jan;145(1):335-344).
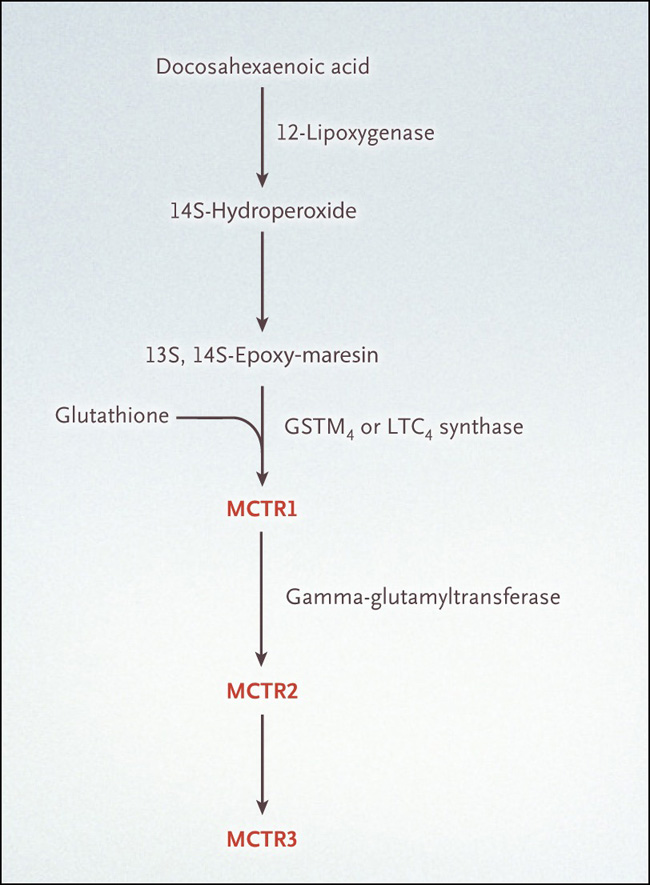
Figura 1. Biosíntesis de MCTR.
Las maresinas se generan dentro de los macrófagos, y sus conjugados peptídicos se generan a través de la acción de la glutatión S-transferasa μ4 (GSTM4) o la leucotrieno C4 [LTC4] sintasa. La GSTM4 tiene una mayor afinidad por la 13S,14S-epoxi-maresina, mientras que la sintasa LTC4 tiene una mayor afinidad por la LTA4. Los conjugados de la maresina en la regeneración de tejidos (MCTR1) pueden ser convertidos aún más por la gamma-glutamiltransferasa a MCTR2, que puede ser convertida por una dipeptidasa a MCTR3. Los resultados de un estudio notificado recientemente por Bruce Levy y sus colegas (J Allergy Clin Immunol. 2020 Jan;145(1):335-344) demuestran que MCTR1, MCTR2 y MCTR3 están presentes en un modelo de ratón de asma y en tejido pulmonar humano.
Los análisis metabolipidómicos del tejido pulmonar humano sano revelaron la presencia de MCTR1, MCTR2 y MCTR3 además de los clásicos cisteinil leucotrienos. En el tejido pulmonar sano, la relación entre los conjugados de sulfuroso SPM - MCTR, PCTR (un péptido conjugado de protectina) y RCTR (un péptido conjugado de resolvina) - y los cisteinil leucotrienos era aproximadamente de 10:3. Por el contrario, en las muestras de tejido pulmonar enfermo, la proporción se invirtió, en aproximadamente 1:10. El análisis del tejido pulmonar humano en cultivo ex vivo mostró la presencia de MCTR1 y su conversión a MCTR2 y MCTR3. Los autores modelaron la contracción de las vías respiratorias en el asma exponiendo rebanadas de tejido pulmonar humano al leucotrieno D4 in vitro. El MCTR3 atenuó significativamente la contracción de las vías respiratorias en respuesta al leucotrieno D4, y una combinación de MCTR1, MCTR2 y MCTR3 atenuó la resistencia al flujo de aire provocada por la exposición al leucotrieno D4 (figura 2), un efecto que fue parcialmente bloqueado por montelukast.
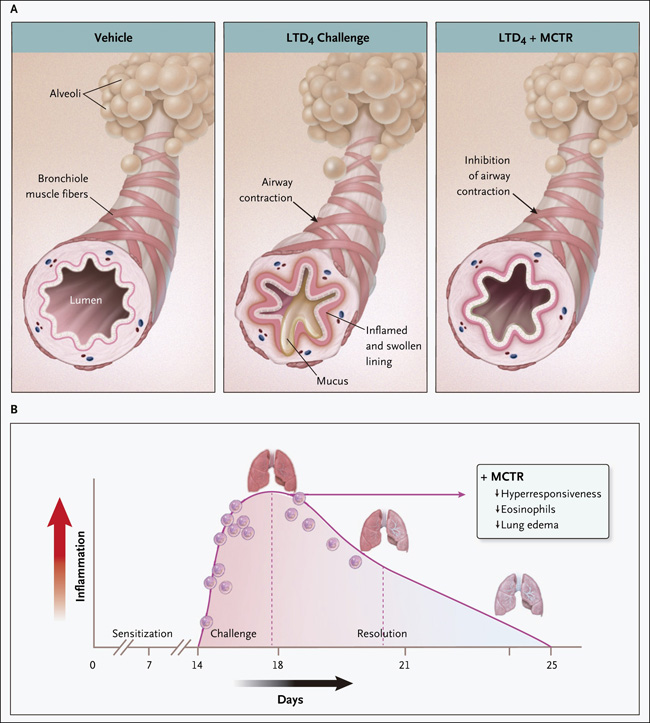
Figura 2. MCTR y respuesta a los cisteinil leucotrienos en el pulmón.
Estimulación del tejido pulmonar humano con LTC4, ex vivo, contracción inducida de las vías respiratorias y reducción del flujo de aire. Estas respuestas fueron inhibidas por los MCTR (panel A). En un modelo de ratón de inflamación alérgica pulmonar, se detectaron distintos perfiles de lípidos en la base, en el pico de la inflamación y en el inicio de la resolución (panel B). En el pico de la inflamación (definido por la acumulación máxima de eosinófilos y citoquinas), se detectaron cisteinil leucotrienos y MCTR (junto con protectores y resolvinas conjugados con sulfuros). A medida que se resolvió la inflamación, los niveles de cisteinil leucotrienos disminuyeron y los niveles de MCTR aumentaron. La adición de MCTR exógena en el pico de la inflamación protegió contra la hiperreactividad de las vías respiratorias, la metaplasia de la mucosa epitelial, la eosinofilia, el aumento de los niveles de albúmina en el líquido de lavado broncoalveolar, un elevado recuento de células en el mismo componente y niveles elevados de IgE en suero. Panel B adaptado desde Bruce Levy y sus colegas (J Allergy Clin Immunol. 2020 Jan;145(1):335-344)
Levy y sus colegas realizaron un análisis metabololipidómico del tejido de los pulmones de los ratones al inicio, en el pico de la inflamación (causado por la alergia de las vías respiratorias inducida por la ovoalbúmina) y durante la resolución. Los MCTR se detectaron en la fase de resolución, al igual que los mediadores conjugados con sulfuros, protectina y resolvina, aunque estos últimos eran menos abundantes que los MCTR.
En el contexto de la biología pulmonar, las principales conclusiones de esta labor son que las actividades de los cisteinil leucotrienos, mediadores establecidos de la inflamación (y objetivo de los medicamentos para el tratamiento del asma), pueden ser moduladas por mediadores de los cisteinil lípidos generados endógenamente, caracterizados por la familia de los MCTR, promoviendo la resolución de la inflamación y atenuando la hiperreactividad y el compromiso de la barrera mucosa. El equilibrio entre (o el predominio relativo de) estas diferentes clases de mediadores refleja la disponibilidad de sustrato y las variadas interacciones entre las transferencias de glutatión S. Levy y sus colegas demostraron que montelukast bloquea parcialmente las respuestas a los MCTR, lo que puede explicar parte de la heterogeneidad de la respuesta clínica a este fármaco y a otros antagonistas de los receptores de cisteinil leucotrieno. Dada la mayor sensibilidad de las personas con asma a los cisteinil leucotrienos y la eficacia de las enzimas para estimular su generación (o, alternativamente, la generación de MCTR), será interesante ver si existen asociaciones entre los polimorfismos de los genes que codifican estas enzimas y el riesgo de asma o su respuesta al tratamiento.
Las respuestas a los cisteinil leucotrienos no se limitan al pulmón. Los receptores de cisteinil leucotrienos se expresan en numerosas células y tejidos y se han propuesto como objetivos terapéuticos en enfermedades cardiovasculares, lesiones de reperfusión relacionadas con la isquemia y fibrosis. Hasta la fecha, la identificación y caracterización de las respuestas a los MCTR indican una mejora en la defensa del huésped, la regeneración y reparación. Por lo tanto, parece prudente evitar bloquear las respuestas a estos reguladores endógenos de la inflamación. En términos más generales, el trabajo de los investigadores se suma a la creciente evidencia de un equilibrio entre la inflamación y las señales que promueven su resolución en condiciones fisiológicas. Destaca, como estrategia terapéutica experimental, el agonismo de resolución como alternativa al antagonismo de la inflamación.
Fuente bibliográfica
Balancing the Effect of Leukotrienes in Asthma
Catherine Godson, Ph.D.
Diabetes Complications Research Centre, Conway Institute and School of Medicine, University College Dublin, Dublin, Ireland.
DOI: 10.1056/NEJMcibr2000118