El Nobel por una gran investigación
El Premio Nobel de Fisiología o Medicina 2021 fue otorgado a David Julius y Ardem Patapoutian por identificar las moléculas que transmiten las sensaciones de la capsaicina. De este modo, proporcionaron los primeros conocimientos sobre cómo los animales perciben las temperaturas frías y calientes, la fuerza mecánica y lo picante.
Todo el mundo está familiarizado con el ardor de un ají. La capsaicina es la sustancia química que produce esta sensación y una respuesta fisiológica al calor, es decir, sudoración intensa. Ahora se sabe que ella activa un receptor en las neuronas sensoriales; esto a través de un minucioso trabajo que llevó a David Julius y colegas a determinar este receptor. No había genomas completos, por lo que el grupo utilizó un enfoque conocido como cribado de expresión para identificar el receptor de capsaicina (figura 1A). Este trabajo implicó aislar una gran cantidad de genes expresados de neuronas sensoriales, transfectar a estos genes a una línea celular humana y luego exponer las células a la capsaicina. Lo que observaron a continuación fue fundamental: un pequeño número de células emitía una señal de calcio en respuesta a la capsaicina añadida. El receptor fue expresado por uno de los genes del acervo genético. Luego, los investigadores probaron cada gen, uno por uno, y finalmente identificaron el receptor que buscaban. Este estaba codificado por un solo gen, un golpe de suerte. Si se hubieran requerido múltiples genes para producir un receptor funcional, este enfoque de cribado habría fallado.
Con receptor en mano, hicieron un hallazgo inesperado. El receptor fue activado no solo por la capsaicina sino también por las temperaturas que los humanos perciben como ardientes. Con este singular descubrimiento se resolvió el antiguo misterio de por qué los ajíes provocan sensación de ardor. Los estudios en ratones knockout confirmaron que este receptor, un canal iónico conocido como TRPV1 (miembro 1 de la subfamilia V del canal receptor de catión de potencial transitorio), era necesario para la detección tanto de capsaicina como de calor nocivo.
Este hecho también proporcionó nueva información sobre la termorregulación, un proceso que utilizan los animales para regular la temperatura corporal. Comer alimentos picantes que contienen capsaicina hace que los humanos suden (una respuesta fisiológica al calor), lo que enfría el cuerpo. Los ratones también se enfrían cuando se les inyecta capsaicina, pero se descubrió que los animales carentes de Trpv1 funcional no se enfriaron cuando se les inyectó la sustancia. Así, la investigación reveló que la activación de TRPV1 estaba directamente acoplada a un proceso homeostático esencial para la supervivencia.
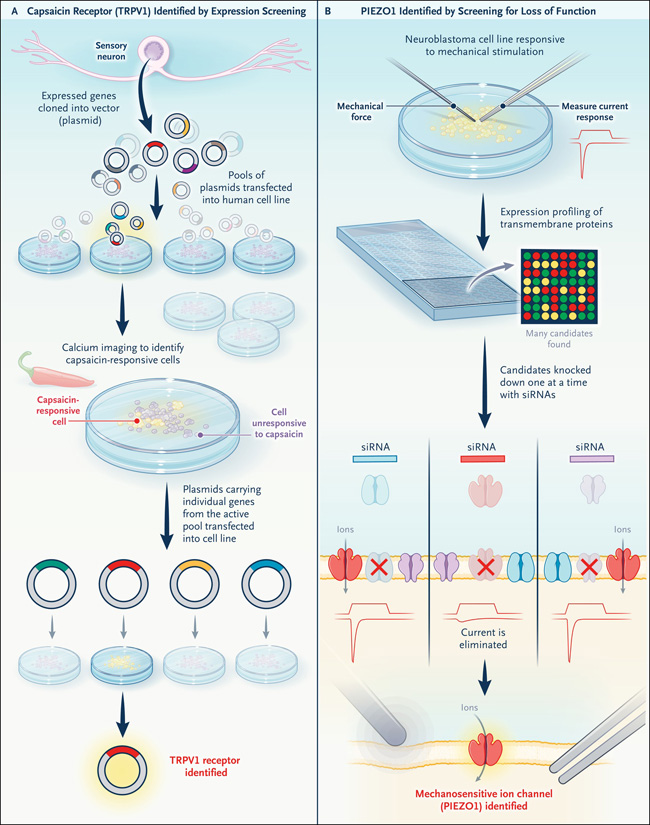
Figura 1: uso de pantallas funcionales para identificar receptores de temperatura y tacto.
El panel A muestra cómo se identificó el receptor de capsaicina (TRPV1 [miembro 1 de la subfamilia V del canal receptor de catión de potencial transitorio]) mediante el cribado de la expresión. Se aislaron conjuntos de genes expresados a partir de neuronas sensoriales, se clonaron en un vector de expresión y luego se transfectaron en una línea celular humana. Se utilizaron imágenes de calcio para identificar las células que respondían a la capsaicina. Uno de los grupos mostró actividad, y se probaron genes individuales para identificar el receptor de capsaicina. El laboratorio de Julius utilizó una estrategia similar para identificar el receptor TRPM8 activado por mentol y frío (miembro 8 de la subfamilia M del canal receptor de catión de potencial transitorio). Casi al mismo tiempo, el grupo de Patapoutian identificó TRPM8 mediante búsquedas de similitud de secuencia en relación con los canales receptores del potencial transitorio (TRP). El panel B muestra cómo se identificó PIEZO1 mediante el cribado de pérdida de función. Se determinó una línea celular que respondía a la deformación mecánica, y luego se identificaron proteínas transmembrana en esta línea celular mediante el perfil de expresión. Estos genes fueron silenciados uno a la vez, lo que condujo a la identificación de PIEZO1 como la proteína mecanosensible. El término ARNip denota ARN interferente pequeño.
El trabajo permitió reconocer los receptores que detectan temperaturas en todo el rango fisiológico. Luego, describieron canales de receptores de potencial transitorio (TRP) que detectan temperaturas frías, así como el agente refrescante mentol (detectado por el receptor TRPM8 [subfamilia M miembro 8 del canal catiónico TRP]), temperaturas cálidas (detectadas por TRPV3 [Miembro 3 de la subfamilia V del canal catiónico TRP) y temperaturas frías nocivas (detectadas por TRPA1 [miembro 1 de la subfamilia A del canal catiónico TRP]). El TRPA1 también es activado por el aceite de mostaza, el formaldehído y los gases de escape del diesel que producen una sensación de ardor o escozor, similar a la forma en que lo hacen las cosas frías.
TRPA1 ha desempeñado diferentes roles a lo largo de la evolución. Sus genes existen en muchas especies, incluidas moscas, mosquitos y serpientes venenosas. Los mosquitos y las serpientes venenosas parecen usar versiones de TRPA1 para comportamientos de búsqueda de calor infrarrojo. Julius y Patapoutian transformaron así nuestra comprensión de cómo las diversas especies detectan la temperatura a nivel molecular. Además, sus descubrimientos insinúan que se podría apuntar a estos receptores farmacológicamente para tratar el dolor crónico y otros trastornos en los que se ve afectada la sensibilidad a los estímulos térmicos.
Patapoutian se enfocó en la mecanosensación; la forma en que los animales detectan los estímulos mecánicos, o la fuerza, área en gran parte desconocida. Su grupo comenzó probando varias líneas celulares con el objetivo de identificar una que respondiera cuando se le pinchara con un estímulo mecánico (figura 1B). Luego identificaron 73 proteínas transmembrana que se expresaron en esta línea celular y eliminaron cada una, identificando finalmente a PIEZO1 como el canal mecanosensible. Este experimento condujo a una cascada de importantes descubrimientos. Las proteínas PIEZO son directamente mecanosensibles y funcionan como canales iónicos. Los estudios posteriores de Patapoutian y colaboradores revelaron roles críticos para los canales PIEZO en muchos procesos mecanosensibles, incluido la sensación táctil, la inflación de los pulmones, la detección de la presión arterial y la detección de la plenitud y el estiramiento de la vejiga.
Las mutaciones que afectan al TRP termosensible y los canales PIEZO mecanosensibles están vinculadas a trastornos y enfermedades sindrómicos, subrayando la importancia clínica de los descubrimientos seminales de Julius y Patapoutian. Además, múltiples compañías farmacéuticas, con miras al desarrollo de nuevos analgésicos, produjeron antagonistas de TRPV1 altamente selectivos. Varios de estos medicamentos se probaron en ensayos clínicos, pero no avanzaron debido a los efectos adversos. La sensibilidad al calor nocivo se redujo en personas tratadas con antagonistas de TRPV1; sin embargo, algunas de estas luego se escaldaron al bañarse o al tomar bebidas calientes. El bloqueo de este sensor de calor también provocó escalofríos en algunos individuos y activó una respuesta de calentamiento homeostático que provoca una hipertermia potencialmente peligrosa. Estos estudios clínicos mostraron que existen riesgos asociados con la focalización global en un receptor que integra la sensación periférica con respuestas fisiológicas, y sugieren que la focalización local de estos tipos de receptores podría ser una opción más segura. Sin embargo, no hay duda de que estos descubrimientos abrieran ventanas para comprender los procesos homeostáticos que son esenciales para la supervivencia; en sensaciones que impulsan percepciones poderosas, como placer, malestar y dolor.
Fuente bibliográfica
A Nobel Prize for Sensational Research
Mark J. Zylka, Ph.D.
UNC Neuroscience Center, University of North Carolina at Chapel Hill, Chapel Hill.
DOI: 10.1056/NEJMcibr2116227