Enfoque genómico para personalizar la oncoterapia
La complejidad genómica es un sello distintivo de muchos tipos de cáncer. Dentro de ésta, la identificación de alteraciones específicas del ADN para las que se dispone de opciones terapéuticas ha abierto la puerta a una nueva era de tratamiento impulsado por los avances genómicos. Las terapias específicas aprobadas se utilizan para una larga lista de alteraciones oncológicas, sobre la base de que los tratamientos ajustados por genotipo tumoral producen mejoras en tiempos de supervivencia y respuesta (disminución del tamaño del tumor). Sin embargo, existe una necesidad permanente de encontrar coincidencias terapéuticas para otras alteraciones genómicas no comprobadas asociadas al cáncer. En un estudio publicado recientemente en Nature, Gary Middleton y colaboradores de la Universidad de Birmingham (Reino Unido) informan resultados de un ensayo clínico utilizando un marco denominado “ensayo umbrella” que tuvo la finalidad de buscar tratamientos farmacológicos ajustados. En este tipo de estudio, bajo el "paraguas" de un único tipo de cáncer -el de pulmón en este caso- se investiga la eficacia de diferentes terapias dirigidas en distintos brazos, cada uno correspondiente a un subconjunto tumoral que alberga alteraciones genómicas específicas.
Terapia ajustada
Una reciente investigación llevada a cabo por Middleton y colaboradores parte del Ensayo Nacional de la Matriz Pulmonar (National Lung Matrix Trial) se centró en el estudio de los cánceres de pulmón de células no pequeñas de 5.467 personas en el Reino Unido (DOI: 10.1038/s41586-020-2481-8). Las muestras de cáncer fueron analizadas para detectar alteraciones genómicas asociadas al tumor que pudieran ser asignadas a uno de los 22 brazos del ensayo. Si se identificaba una alteración, las personas podían ser asignadas a una terapia específica. Cada par de terapia para una alteración determinada se eligió sobre la base de los datos preclínicos de estudios de laboratorio que apoyaban el emparejamiento. Se comunicaron datos de 288 pacientes (14% de la población elegible que fue emparejada con una terapia), que representaban 19 de los 22 brazos. Los autores utilizaron un método estadístico denominado análisis bayesiano para evaluar los resultados clínicos. Esto separó los resultados del ensayo en dos grupos, dependiendo del éxito de los resultados del tratamiento.
Los del primer grupo fueron emparejamientos exitosos. Ciertos tratamientos ajustados dieron como resultado altas tasas de respuesta (más del 60% de las personas tratadas tuvieron una reducción sustancial del tumor) y una supervivencia duradera sin progresión (sin signos de crecimiento del tumor durante más de 12 meses). Por ejemplo, el fármaco osimertinib, que inhibe al receptor del factor de crecimiento epidérmico (EGFR), fue exitoso para los cánceres de pulmón asociados a una alteración de un residuo de aminoácido de treonina a metionina (T790M) en el EGFR. El fármaco crizotinib, que inhibe determinadas proteínas receptoras, incluidas la ROS1 y MET, proporcionó un tratamiento eficaz (figura 1) para los tumores con anomalías en cualquiera de los genes codificantes para estas proteínas. Estos resultados son coherentes con datos clínicos previos, que han conducido a la aprobación o recomendación de estas terapias dirigidas molecularmente en directrices nacionales de tratamiento. Los resultados de Middleton y sus colegas confirman el poder de estas mutaciones para predecir los resultados terapéuticos y también destacan el efecto transformador de la medicina personalizada basada en el genoma en la atención oncológica. El éxito de algunos enfoques personalizados ha impulsado la creciente adopción de la secuenciación del ADN para identificar los cambios genómicos que luego dirigen los tratamientos de precisión en la práctica rutinaria.
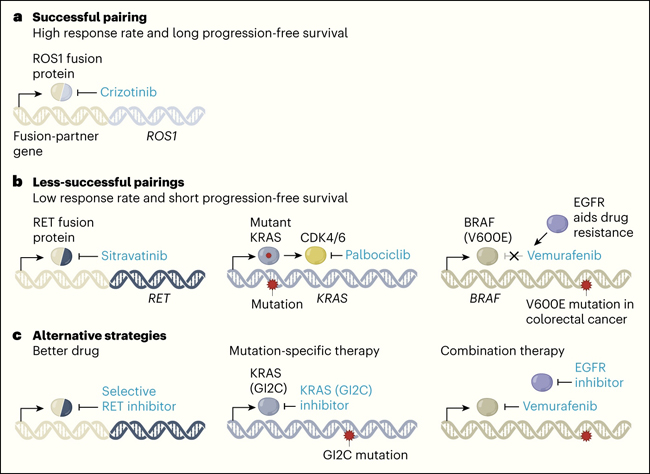
Figura 1 | Tratamiento del cáncer a medida.
Gary Middleton y colaboradores informan de los resultados de un ensayo clínico con personas con cáncer de pulmón (DOI: 10.1038/s41586-020-2481-8). Si los individuos tenían alteraciones en el ADN para las cuales las pruebas de laboratorio indicaban que había una terapia farmacológica efectiva, recibían un tratamiento ajustado a su genotipo tumoral. a, Algunos emparejamientos terapéuticos fueron exitosos. Por ejemplo, el fármaco crizotinib trató eficazmente a personas cuyo gen ROS1 se había fusionado con otro gen. Sus tumores se redujeron y tuvieron una supervivencia sin progresión a largo plazo. b, Sin embargo, la mayoría de los ajustes tuvieron menos éxito. Los emparejamientos ineficaces incluían el uso del fármaco sitravatinib en personas cuyo gen RET se había fusionado con otro gen, o el tratamiento con palbociclib para inhibir la activación anormal de las proteínas CDK4 y CDK6 que surge en individuos que tienen una versión mutante de la proteína KRAS. Algunos emparejamientos podrían haber fallado porque otra proteína ayudó a la resistencia a los medicamentos. Por ejemplo, en el cáncer colorrectal, se sabe que la proteína EGFR impide que el fármaco vemurafenib se dirija eficazmente a una proteína BRAF que tiene una mutación V600E6. c, Para dirigirse a los tumores que tuvieron emparejamientos menos exitosos, cambiar a otras estrategias, como los ejemplos que se muestran, puede ofrecer un camino a seguir.
En comparación, los resultados fueron menos satisfactorios en el segundo grupo. Se observaron tasas de respuesta inferiores al 10% y tiempos cortos de supervivencia sin progresión en la mayoría de los tipos de tratamientos probados. Varios brazos de prueba fueron abandonados porque eran ineficaces. En los cánceres con mutaciones asociadas con alteraciones en la progresión del ciclo celular, el tratamiento con un fármaco que inhibe las enzimas clave del ciclo celular, CDK4 y CDK6, logró sólo una tasa de respuesta del 1%. La tasa de respuesta fue del 3% en los cánceres con alteraciones en la vía de señalización de PI3K tratados con inhibidores de las proteínas mTOR o AKT, que actúan en esta vía. Se encontró una tasa de respuesta baja, de 7%, en los cánceres con alteraciones en otra vía de señalización, la vía del RAS, que fueron manejados con inhibidores de proteínas activadas por RAS (MEK, mTOR o CDK4/6).
La tasa de respuesta más alta en este segundo grupo fue 31% (muy por debajo de las tasas de respuesta de al menos 60% en el primer grupo) para los cánceres con pérdida del gen NF1. La pérdida de este gen resulta en la activación de MEK, y estos tumores fueron tratados con inhibidores de MEK. Sin embargo, este tratamiento se combinó con quimioterapia, lo que confundió los esfuerzos en evaluar el contribuyente dominante a la respuesta.
La elección de la alteración genómica apropiada al tomar una decisión de orientación es una consideración igualmente crucial. Pueden existir variaciones sustanciales en las alteraciones encontradas en un gen mutado determinado. Por ejemplo, las mutaciones en el gen KRAS examinado en este ensayo son notablemente diversas. Se sabe que un cambio particular del aminoácido glicina a cisteína (G12C) en la proteína KRAS ofrece un objetivo farmacológico que puede tratarse con inhibidores selectivos de G12C de KRAS. Estos agentes ya han logrado una actividad clínica sin precedentes contra estas alteraciones previamente “no tratables farmacológicamente”.
Se pueden considerar otros diseños para optimizar la eficiencia de un ensayo. Un ensayo general limita la evaluación del tratamiento a un solo tipo de tumor. Por el contrario, en lo que se denominan ensayos en cesta, los participantes reciben una terapia independientemente de su tipo de cáncer, siempre y cuando el cáncer tenga la alteración genómica de interés. Los primeros ensayos en cesta se limitaban a un único par de terapia y alteración. Pero en los diseños de ensayos más recientes, se ofrecen diversas opciones de tratamiento que se ajustan a la variedad de alteraciones detectadas durante el análisis de ADN, lo que permite que participen más personas.
El National Lung Matrix Trial es un esfuerzo impresionante. Demuestra bien la viabilidad de la secuenciación integral del genoma del cáncer y la administración de varias intervenciones terapéuticas dirigidas molecularmente en un solo ensayo. También pone de manifiesto la capacidad de esos programas para prestar con éxito atención sanitaria contra el cáncer como parte de un sistema en el que participan muchos grupos de interesados diferentes: pacientes, grupos de defensa del paciente, personas que trabajan en diagnóstico, investigadores académicos y personas de la industria farmacéutica. Los futuros ensayos de este tipo deberían centrarse en medidas como la realización de pruebas más tempranas y la iniciación del tratamiento, lo que podría aumentar la proporción de personas aptas que reciben tratamiento. El ensayo no fue diseñado para obtener aprobaciones oficiales de medicamentos. Un ensayo diseñado teniendo en cuenta la aprobación del fármaco maximizaría los esfuerzos de los interesados, en particular si se ampliara para incluir a múltiples países.
¿Cómo deberíamos avanzar en la atención sanitaria anticancerígena impulsada por el genoma en esta década? Los protocolos del futuro deberían imitar los ágiles atributos de los cánceres que se intentan tratar. La adaptación y evolución de diversos enfoques para lograr plataformas de ensayo muy flexibles, globales y centradas en la reglamentación permitirán que la ciencia clínica siga siendo ágil y pertinente en medio de arenas en constante cambio.
Fuente bibliográfica
An umbrella approach to test lung cancer therapies
Alexander Drilon & Matthew D. Hellmann
Department of Medicine, Weill Cornell Medical College, New York.
d41586-020-02062-5