Nuevo paradigma contra enemigos infecciosos
La inmunidad adaptativa proporciona una protección de por vida al generar de memoria central, efectoras y las más recientemente descritas células T de memoria residente en tejido (TRM). Sin embargo, el origen celular de linfocitos CD4 TRM y su contribución a la defensa del huésped siguen siendo difíciles de determinar. Utilizando modelos de ratones con seguimiento de destino de IL-17A, se evidenció que una fracción significativa de las células CD4 TRM pulmonares derivan de las células efectoras productoras de IL-17A (TH17) después de la inmunización con Klebsiella pneumoniae (Kp) eliminada por calor. Estas células TRM exTH17 se mantienen en el pulmón por la IL-7, producida por las células endoteliales linfáticas. Durante una respuesta de memoria, ni los anticuerpos, las células T γδ, ni linfocitos T circulantes son suficientes para la rápida defensa del huésped requerida para eliminar la Kp. Por el contrario, usando estudios de agotamiento, se demostró que las células exTH17 TRM juegan un papel importante en la eliminación bacteriana. DE esta forma, se determinó el origen y la función de las células TRM CD4 de las vías respiratorias durante la infección bacteriana, ofreciendo nuevas estrategias para afrontar infecciones complejas y sepsis.
Evitando la inmunosupresión
El descubrimiento de los antibióticos es quizás el avance más importante de la medicina en el siglo pasado. Sin embargo, la aparición de patógenos multirresistentes a los medicamentos ha hecho que muchos antibióticos sean ineficaces y está alimentando una crisis: un aumento espectacular de la incidencia de infecciones refractarias al tratamiento, lo que causó más de 35.000 muertes en los Estados Unidos en 2019. Afortunadamente, también está aumentando el conocimiento de los mecanismos celulares de la inmunidad, incluidos los que están sustentados por subclases de células T. Estudios recientes de Amezcua Vesely y colaboradores (Cell 2019;178(5):1176-1188.e15) y Ryan Zander y colegas (Immunity 2019;51(6):1028-1042.e4) aumentan este conocimiento y apoyan el desarrollo de medicamentos que refuerzan la inmunidad en pacientes con infecciones que ponen en peligro su vida.
Hasta hace relativamente poco tiempo se consideraba que la muerte en el contexto de la sepsis era el resultado de una hiperinflamación mediada por una tormenta de citoquinas, pero trabajos posteriores revelaron que esta explicación era inadecuada. Los avances en las terapias de apoyo han disminuido notablemente las muertes durante las primeras fases del shock séptico; en la gran mayoría de los pacientes supervivientes se produce una inmunosupresión prolongada después de la fase inflamatoria inicial. El efecto de la inmunosupresión se manifiesta en la incidencia de nuevas infecciones secundarias, a menudo debidas a patógenos poco virulentos, que se producen en un 30 a 40% de los pacientes con sepsis prolongada. Otras pruebas del papel fundamental de la inmunidad del hospedero en la supervivencia de la sepsis son las características de los pacientes que mueren: pacientes mayores, en los que se sabe que la inmunosenescencia es prevalente, y pacientes que tienen alcoholismo, están desnutridos o tienen cáncer o afecciones coexistentes graves que dañan el sistema inmunitario. La reactivación de múltiples virus latentes que se produce en el 50% de los pacientes con sepsis prolongada ilustra aún más su grave inmunosupresión.
Los linfocitos T invariantes asociados a la mucosa (MAIT, por sus siglas en inglés) y las células T gamma/delta (células T γδ) son linfocitos de tipo innato que recubren la mucosa bronquial y responden rápidamente a la invasión de patógenos secretando citoquinas esenciales para la eliminación de microbios: interferón-γ e interleucina-17. Vesely y sus colegas han añadido a este grupo las células T CD4 de memoria residentes en tejido (CD4 TRM): descubrieron están presentes en el pulmón y se derivan de las células efectoras TH17 (que secretan interleucina-17) y que eliminan las bacterias, incluida la Klebsiella pneumoniae resistente al carbapenem, en modelos de infección de ratones. Determinaron además que la interleucina-7 era necesaria para el mantenimiento de estas células CD4 TRM en el pulmón. Zander y colaboradores informaron de un nuevo papel de apoyo de las células T CD4 que producen interleucina-21: estimulan la generación de un subconjunto de células T CD8 que eliminan las células infectadas por virus en un modelo de ratón de infección viral latente.
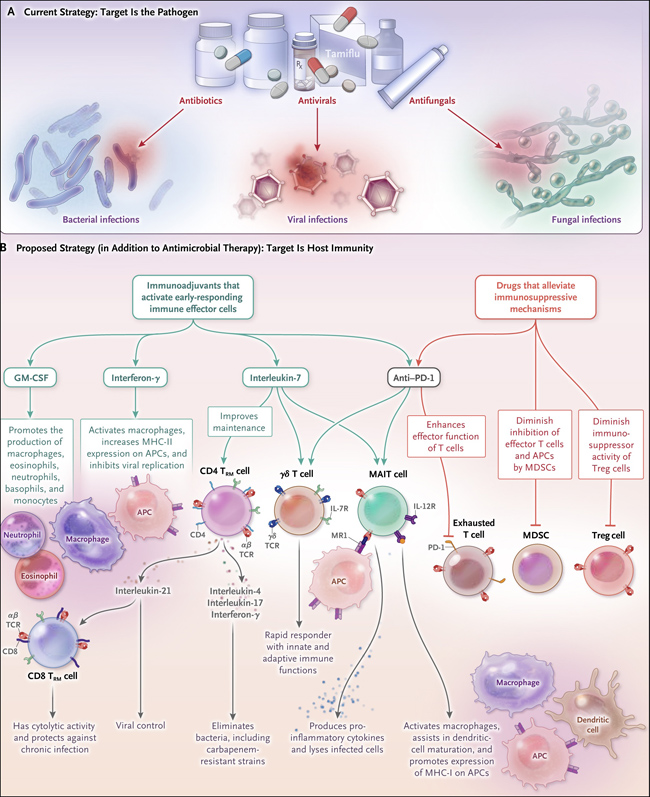
Figura 1. Nuevo paradigma terapéutico en enfermedades infecciosas.
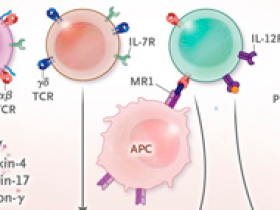
La actual estrategia general para tratar las enfermedades infecciosas (recuadro A) consiste en la rápida administración de medicamentos antimicrobianos dirigidos a patógenos. En el futuro (recuadro B), es probable que, además de los agentes antimicrobianos, se utilicen inmunoadyuvantes que activen células inmunitarias efectoras de respuesta temprana (flechas verdes) o que atenúen los mecanismos inmunosupresores (líneas rojas). Las células T invariantes asociadas a la mucosa (MAIT) y las células T γδ responden rápidamente para eliminar los patógenos invasores. En estudios recientes se identificaron nuevas clases adicionales de células efectoras inmunitarias de respuesta temprana, incluidas las células T CD4 y CD8 de memoria residente en el tejido (CD4 TRM y CD8 TRM) que desempeñan funciones clave en la defensa del hospedero. El agotamiento de las células T, las células supresoras derivadas de mieloides (MDSC) y linfocitos T reguladores (Treg) son fuentes importantes de inmunosupresión en pacientes con infecciones prolongadas, incluida la sepsis. La interleuquina-7, agentes anti PD1, el interferón-γ, y el factor estimulante de colonias de granulocitos-macrófagos (GM-CSF) son inmunoadyuvantes que se han utilizado de forma compasiva en pacientes con infecciones bacterianas, fúngicas y virales que ponen en peligro la vida y en pequeños ensayos clínicos de individuos con sepsis. La interleuquina-7 y anti-PD-1 activan linfocitos T, células MAIT y a las γδ. La interleuquina-7 además apoya a las células CD4 TRM. El bloqueo de PD-1 se usa para revertir el agotamiento de linfocitos T. APC denota célula presentadora de antígenos; 7 IL-7R, receptor de interleucina; IL-12R, receptor de interleucina-12; MH-I, complejo de histocompatibilidad mayor clase I; MHC-II, complejo de histocompatibilidad mayor clase II; MR1, proteína relacionada con el complejo de histocompatibilidad mayor clase I; y TCR receptor de células T.
Estos estudios tienen implicaciones para el desarrollo de terapias inmunoadyuvantes experimentales (figura 1). En los últimos años se han realizado ensayos de fase 1 y 2 del factor estimulante de colonias de granulocitos-macrófagos, el interferón-γ, agentes antiproteína de muerte programada 1 (PD-1), anti ligando de proteína de muerte programada 1 (PD-L1) e interleucina-7 en pacientes con sepsis. Aunque los ensayos fueron pequeños, los resultados indicaron que los medicamentos tenían perfiles de seguridad satisfactorios, no inducían tormenta de citoquinas y mejoraban los índices de inmunidad de los pacientes. Además, hay un número creciente de informes de casos que documentan mejoras clínicas en pacientes que reciben agentes inmunoadyuvantes para el tratamiento de infecciones por patógenos que ponen en peligro la vida, como el virus JC (el agente etiológico de la leucoencefalopatía multifocal progresiva), el virus de la hepatitis C, el Staphylococcus aureus, la candidiasis diseminada y la mucormicosis. Varios de estos inmunoadyuvantes activan las células inmunitarias de respuesta rápida, incluyendo las células CD4 TRM, las MAIT y las células T γδ. En conjunto, estos estudios sugieren que las terapias inmunoadyuvantes podrían probarse experimentalmente como tratamiento para infecciones que de otro modo serían intratables, incluyendo aquellas que ocurren en el contexto de la sepsis.
Hasta hace poco, la mayoría de los ensayos que estudiaban formas de potenciar la inmunidad en pacientes con sepsis se centraban en los neutrófilos y monocitos, pero no en las células T. El sistema inmunitario es como una orquesta que funciona mejor cuando todos los componentes trabajan en armonía; por esta analogía, la célula T colaboradora (helper) CD4 es la directora. La importancia de la orientación de las células T para una respuesta inmunológica eficaz queda demostrada en oncología: los inhibidores de punto de control que invierten el agotamiento de linfocitos T son las actuales "superestrellas" oncológicas y se incluyen en la mayoría de los ensayos de inmunoterapia en curso. El notable poder de las células T se pone de relieve con la aprobación de los fármacos anti-PD-1 y anti-PD-L1 para tratar más de 10 tipos de tumores muy diversos. La interleuquina-7, que se está probando actualmente en varios ensayos oncológicos, activa no solo las células T CD4 y CD8, sino también las células MAIT y las T γδ. Predecimos que las terapias de combinación de fármacos también se convertirán en el estándar para la sepsis.
Entonces ¿qué se necesita hacer? Hay más de 1700 ensayos de inmunoterapia en curso en oncología, mientras que casi ningún ensayo con pacientes con sepsis está en marcha. Lo más importante es que los líderes farmacéuticos y de los Institutos Nacionales de Salud necesitan visión y coraje para apoyar los ensayos que refuerzan la inmunidad del huésped en las enfermedades infecciosas, incluida la sepsis. Los fracasos de los medicamentos que se probaron en ensayos anteriores sobre sepsis, casi todos ellos concebidos para bloquear la hiperinflamación mediada por citoquinas, probablemente se basaron en ideas erróneas sobre los mecanismos subyacentes al trastorno. Un escepticismo intenso similar con respecto a la inmunoterapia impregnó el campo de la oncología hasta el éxito espectacular de los inhibidores de los puntos de control. Los candidatos ideales para las terapias inmunoadyuvantes son los pacientes con infecciones adquiridas en el hospital, infecciones con bacterias multirresistentes o infecciones por hongos. Estos pacientes casi siempre tienen inmunosupresión, y la mortalidad entre estos pacientes es alta. Si la inmunoterapia resulta ser un tratamiento eficaz, podría servir como arma contra enemigos cada vez más letales.
Fuente bibliográfica
Activating Immunity to Fight a Foe — A New Path
Richard S. Hotchkiss, M.D., and Steven M. Opal, M.D.
Departments of Anesthesiology, Medicine, and Surgery, Washington University School of Medicine, St. Louis.
DOI: 10.1056/NEJMcibr1917242