Oligonucleótidos para vencer la aterosclerosis
Los niveles de lipoproteína(a), una variante de lipoproteína de baja densidad, están determinados genéticamente y, cuando son elevados, constituyen un importante factor de riesgo de enfermedad cardiovascular (ECV) y de estenosis aórtica. Pese a su relevancia clínica, actualmente no hay terapias farmacológicas aprobadas para reducir la concentración sanguínea de lipoproteína(a). Este escenario podría cambiar gracias a un ensayo aleatorizado, doble ciego, controlado por placebo, que evaluó una gama de dosis en 286 pacientes con enfermedad cardiovascular establecida y con niveles de lipoproteínas(a) de al menos 60 mg por decilitro (150 nmol por litro). Los individuos recibieron el oligonucleótido antisentido (ASAO) dirigido a hepatocitos, llamado AKCEA-APO(a)-LRx en dosis de 20, 40 o 60 mg cada 4 semanas o un placebo, por vía subcutánea durante 6 a 12 meses. Como resultado, este tratamiento bajó los niveles de lipoproteína(a) de manera dependiente de la dosis, con una disminución absoluta más notoria en sujetos con la mayor concentración inicial de lipoproteína(a). Esta terapia hipolipemiante en fase de prueba clínica representa un gran paso en la reducción de eventos de ECV aterosclerótica en la población tratada, pero en la que persiste un sustancial riesgo residual debido a los elevados niveles de Lp(a).
Contra la lipoproteína(a)
A pesar del éxito de los fármacos reductores del colesterol de lipoproteínas de baja densidad (LDL-C) para disminuir los episodios de enfermedad cardiovascular (ECV), aún persiste un considerable riesgo residual de complicaciones por ECV aterosclerótica (ECVAT), incluso entre los pacientes tratados de forma agresiva. En los últimos años, el foco de atención de las investigaciones sobre los factores que provocan la ECVAT ha pasado del efecto del LDL-C circulante a la identificación de otros factores contribuyen a la enfermedad aterosclerótica. La lipoproteína(a) (Lp(a)), una molécula proaterogénica en la sangre, cuyos niveles están fuertemente determinados por la genética, ha pasado a primer plano como factor de riesgo causal de la ECVAT y como una diana terapéutica a considerar. En una publicación reciente en New England Journal of Medicine, Tsimikas y colaboradores informaron de los resultados de un ensayo clínico de fase 2 sobre un nuevo oligonucleótido antisentido (ASO, por sus siglas en inglés) dirigido a la biosíntesis de Lp(a) que es capaz de reducir los niveles de Lp(a) hasta en un 80% (N. Engl. J. Med. 382, 244–255 (2020)). Esto debería dar esperanzas a los millones de personas con Lp(a) marcadamente elevada y que corren un alto riesgo de sufrir eventos relacionados con la ECVAT.
La Lp(a) es una lipoproteína inusual producida por el hígado que, al igual que el LDL, contiene lípidos y una molécula de apolipoproteína B, pero también contiene una proteína única conocida como "apolipoproteína(a)" (apo(a)). Los niveles de Lp(a) están muy determinados genéticamente por la variación de LPA (que codifica la proteína apo(a)), pero no están fuertemente influenciados por el estilo de vida, la dieta u otros factores ambientales. Existen grandes diferencias en los niveles de Lp(a) circulantes según la ascendencia, siendo las personas de origen africano las que tienen los niveles más altos y las de procedencia asiática oriental las que tienen los niveles más bajos. Los estudios genéticos a gran escala han confirmado que la Lp(a) es un factor de riesgo causal de la ECVAT: las variantes de LPA asociadas con niveles más altos de Lp(a) también se asocian con un mayor riesgo de enfermedad coronaria, aunque esta relación puede variar según la ascendencia. Los niveles de Lp(a) y las variantes genéticas de LPA también se asocian significativamente con un mayor riesgo de calcificación de la válvula aórtica y de estenosis aórtica. Los mecanismos por los que los niveles elevados de Lp(a) promueven la ECVAT y la estenosis aórtica no están claros, pero la Lp(a) es la principal portadora en sangre de fosfolípidos oxidados proinflamatorios, que pueden tener un papel clave
Un reciente metaanálisis de siete ensayos sobre estatinas controlados por placebo con más de 29.000 pacientes (tanto de prevención primaria como de ECV anteriores) mostró que los niveles iniciales y de Lp(a) con estatinoterapia se asociaban de manera casi lineal con el riesgo de resultados cardiovasculares (CV). Hubo un aumento de más del 40% del riesgo de eventos de ECV en pacientes con niveles de Lp(a) de 50 mg/dl o más, en comparación con el riesgo de aquellos con niveles <15 mg/dl, independientemente de LDL-C y otros factores de riesgo. Por lo tanto, las crecientes pruebas apoyan la medición clínica de los niveles de Lp(a) como parte de la evaluación del riesgo de ECV. Si bien la medición de Lp(a) aún no ha sido completamente estandarizada, se estima que ~35 - 40% de la población de los EE.UU. tiene niveles de Lp(a) >30 mg/dl y ~25 - 30% tiene niveles de Lp(a) >50 mg/dl. Los niveles altos de Lp(a) podrían utilizarse para reclasificar a los pacientes de riesgo intermedio en una categoría de alto riesgo, con niveles más elevados de Lp(a) que motiven un tratamiento más agresivo dirigido al LDL-C en estos pacientes. Para los sujetos con ECVAT, la Lp(a) ofrece información pronóstica sobre el riesgo de futuros eventos, incluso después de que se logre un control óptimo de LDL-C y otros factores de riesgo. Además, como factor de riesgo altamente hereditario, podría motivar la evaluación del riesgo y la modificación de los factores en los miembros de la familia.
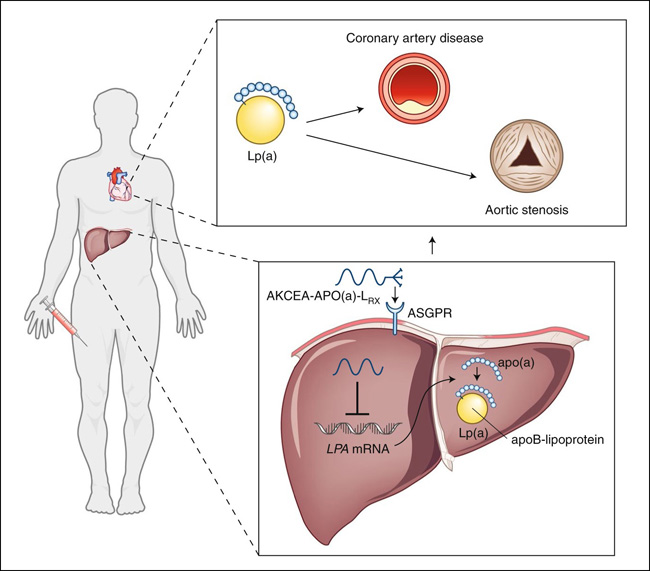
Fig. 1: Un oligonucleótido para la aterosclerosis.
En los hepatocitos, el ARNm de LPA se traduce en la proteína apo(a), que forma un complejo con la apolipoproteína B (apoB) para formar la partícula madura Lp(a). AKCEA-APO(a)-LRx se dirige al ARNm de LPA, lo que conduce a una producción notablemente reducida de la proteína apo(a) y, por lo tanto, reduce la biosíntesis de Lp(a) y sus niveles en la sangre. ASGPR, receptor de la asialoglicoproteína.
Los niveles elevados de Lp(a) no pueden reducirse mediante el estilo de vida o la intervención dietética. Aunque las dosis altas de niacina reducen modestamente los niveles de Lp(a), no logran disminuir sustancialmente los resultados de las ECV cuando se combina con la terapia de estatinas. Los inhibidores de la enzima PCSK9 (de la proproteína convertasa subtilisina-kexina 9) reducen los niveles de Lp(a) en un modesto 20 - 30% a través de un mecanismo que no está claro. En un gran ensayo aleatorizado sobre desenlaces CV con el inhibidor de PCSK9, evolocumab, que mostró una baja significativa de los principales eventos adversos CV, los niveles más altos de Lp(a) se asociaron de forma independiente con los desenlaces CV, los pacientes con niveles iniciales más altos de Lp(a) experimentaron una mayor reducción absoluta de Lp(a) y una mayor reducción de los eventos adversos CV. Además, el grupo que alcanzó los niveles más bajos combinados de LDL-C y Lp(a) experimentó la tasa más baja de eventos adversos. Cabe esperar que una intervención que reduzca sustancialmente la Lp(a) reduzca los eventos adversos CV incluso en pacientes con niveles óptimos de LDL-C.
En el último decenio se ha producido una explosión del interés en los tratamientos con ácidos nucleicos que se dirigen a especies específicas de ARNm. El nuevo ASO AKCEA-APO(a)-LRx apunta a los ARNm que codifican el apo(a) y por lo tanto impide la biosíntesis de las partículas Lp(a) (figura 1). Este fármaco está hecho de N-acetilgalactosamina (GalNAc) conjugada con el ASO y por lo tanto se une al receptor de la asialoglucoproteína en los hepatocitos. Su inyección subcutánea da como resultado una entrega altamente eficiente y específica al hígado, el principal sitio de producción de apo(a) (figura 1). En el estudio de fase 2, recientemente publicado, se incluyó en el ensayo a un total de 286 pacientes con niveles establecidos de ECVAT y Lp(a) inicial de al menos 60 mg/dl, los que fueron asignados al azar para recibir dosis crecientes de AKCEA-APO(a)-LRx o placebo. Los autores encontraron que, en estas personas, hubo una reducción dependiente de la dosis de los niveles de Lp(a), con una reducción del 80% de los niveles de Lp(a) en el grupo asignado aleatoriamente a recibir la dosis más alta (20 mg semanales). Este grupo tenía un nivel medio de inicial de Lp(a) de aproximadamente 98 mg/dl y experimentó una reducción absoluta de Lp(a) de 75 mg/dl. El 98% de los individuos de este grupo de tratamiento alcanzaron un nivel de Lp(a) de <50 mg/dl, lo que indica una respuesta terapéutica altamente efectiva. No se comunicaron problemas importantes de seguridad o tolerabilidad.
Después de décadas de investigación sobre la Lp(a), es emocionante que ahora exista una intervención que reduce notablemente los niveles de Lp(a) y que se esté probando formalmente su capacidad para reducir los eventos adversos CV. La extrapolación de la evidencia epidemiológica, genética y clínica sugiere que el grado de reducción de Lp(a) esperado en el ensayo clínico (~80%) debería producir una reducción sustancial y clínicamente significativa de los eventos de CV. Las terapias de reducción de Lp(a) representan un importante paso adelante en la reducción de eventos de ECV en la población con LDL-C tratada, pero con un riesgo residual sustancial debido a los elevados niveles de Lp(a).
Fuente bibliográfica
Antisense oligonucleotides for atherosclerotic disease
Archna Bajaj & Daniel J. Rader
Perelman School of Medicine, University of Pennsylvania, Philadelphia, PA, USA
Nat Med. 2020 Apr;26(4):471-472