Oocitos generados a partir de células madre
Las células madre murinas demuestran una recapitulación de todo el ciclo de vida de la línea germinal femenina, resultando en ovocitos de ratón fertilizables en cultivo. Entre aproximadamente 200 embriones de dos células transferidos a madres pseudopreñadas, el 5% puede generar crías vivas.
Las células germinales primordiales, que emergen alrededor del día 16 en los embriones humanos tempranos, se desarrollan para formar ovogonios de modo que, finalmente, la cantidad de ovocitos que están presentes en una mujer adulta se fija al nacer. Después de pasar por un programa de desarrollo complejo en las gónadas fetales, las células germinales primordiales crecen para conformar ovogonios, que generar ovocitos capaces de madurar y fertilizarse (figura 1). Recapitular todo el ciclo de vida de la línea germinal femenina con células madre y terminar con ovocitos funcionales en cultivo es una gran tarea, sin embargo, T. Yoshino y colaboradores lo acaban de lograr. Comenzando con células madre embrionarias de ratón, estos investigadores produjeron unidades somáticas de ovario fetal, que apoyaron el desarrollo de células germinales primordiales (también derivadas de células madre embrionarias) en ovocitos capaces de ser fertilizados. Un subconjunto de embriones desarrollados a término.
Las células germinales primordiales y las gónadas progresan de forma independiente en los embriones, por lo que se requiere que las células germinales primordiales migren a las gónadas en desarrollo; esta migración es seguida por el desarrollo sincronizado de las dos entidades, durante el cual las células germinales primordiales proliferan antes de madurar para formar ovogonias. Estas entran en meiosis y eventualmente terminan como ovocitos. La meiosis asegura que cada gameto femenino sea haploide y, por lo tanto, complementará la contribución paterna equivalente en la fertilización. La meiosis y la formación de ovocitos son eventos genéticamente separables, pero la meiosis defectuosa es una barrera para el desarrollo de ovocitos funcionales capaces de transmitir una sola copia de cada cromosoma.
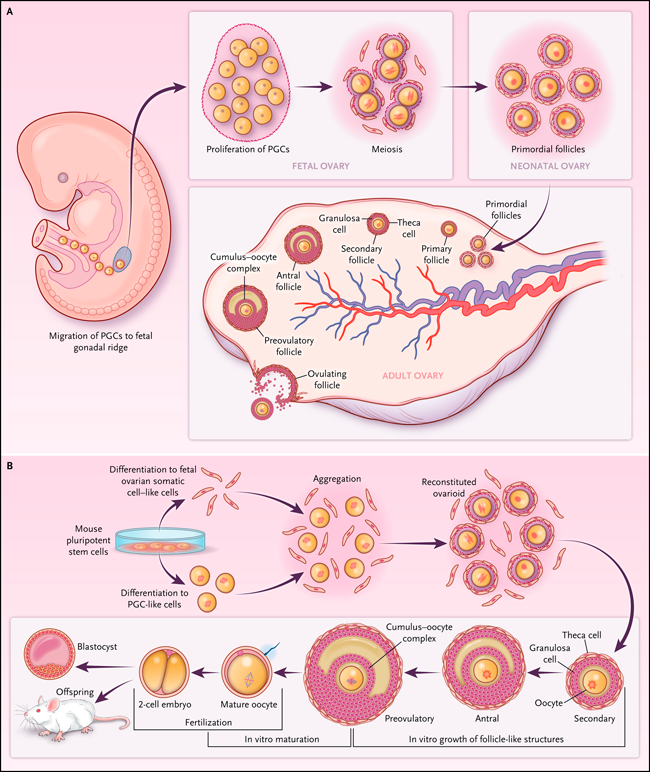
Figura 1: recapitulación del desarrollo de células germinales y somáticas ováricas en la generación de ovocitos funcionales a partir de células madre pluripotentes.
Las células germinales primordiales (PGC) migran a las gónadas en desarrollo y proliferan. Las células somáticas gonadales se diferencian en estroma ovárico, granulosa y células de la teca. Paralelamente, las unidades germinales se diferencian y entran en meiosis, formando ovocitos que, rodeados por una capa de células granulosa, producen folículos primordiales. Después del reclutamiento para el crecimiento, estos se desarrollan hasta la etapa de folículo secundario, que contiene múltiples capas de células de la granulosa rodeadas por células de la teca. En las hembras sexualmente maduras, los folículos se desarrollan en la etapa preovulatoria y los ovocitos reanudan la meiosis y se detienen después de completar la primera división meiótica antes de la ovulación (panel A). En la diferenciación in vitro de células somáticas de ovario y PGC de células madre embrionarias (panel B), la agregación de ovario fetal derivado de células madre embrionarias promueve la proliferación y diferenciación de ambos linajes para formar ovarios reconstituidos. Las estructuras similares a folículos en el ovarioide progresan desde la etapa de folículo primordial hasta folículo secundario. Transferidas a condiciones que promueven el crecimiento, las estructuras secundarias similares a folículos se desarrollan para formar folículos similares a preovulatorios, a partir de los cuales se generan complejos de cúmulos y ovocitos que se recolectan y maduran in vitro. La fertilización de los ovocitos maduros da como resultado embriones viables.
Katsuhiko Hayashi y colegas generaron células somáticas de ovario a partir de células madre embrionarias de ratón en cultivo imitando paso a paso las trayectorias de desarrollo desde el mesodermo hasta el estroma ovárico fetal, la granulosa y las células de la teca que constituyen el folículo ovárico. La agregación de células similares a células somáticas de ovario derivadas de células madre embrionarias con células similares a células germinales primordiales resultó en ovarios reconstituidos. Para el día 3 de cultivo, las células de la granulosa rodeaban las células similares a las células germinales primordiales, promoviendo su proliferación y expresión del marcador tardío de células germinales DDX4. Estructuras similares a cremalleras llamadas complejos sinaptonémicos, en los que los cromosomas homólogos emparejados experimentan una recombinación meiótica, eran evidentes en los núcleos de las células germinales al día 7. A medida que avanzaban los cultivos, las estructuras similares a los folículos quedaron rodeadas por una capa de células similares a la teca. Después de 23 días de cultivo, los ovocitos se rodearon de múltiples capas de células similares a la granulosa para formar estructuras secundarias similares a folículos, que luego se colocaron en condiciones específicas de cultivo que previamente se ha demostrado que favorecen el crecimiento hasta la etapa preovulatoria. Durante 12 días las células de la granulosa proliferaron y formaron complejos cúmulo-ovocitos. Después del cultivo en condiciones de maduración in vitro, 33 de 116 ovocitos (28%) extruyeron un primer cuerpo polar, marcando la finalización de la primera división meiótica.
La fertilización in vitro de ovocitos derivados de células madre maduras fue seguida por el desarrollo hasta la etapa de dos células, y el 26 % de estos embriones progresaron hasta blastocistos. De los 212 embriones de dos células que se trasplantaron en oviductos de madres pseudopreñadas, 11 (5%) dieron crías vivas. El grupo de Hayashi habían obtenido previamente resultados similares en células gonadales fetales de ratón, lo que sugería que sus células gonadales derivadas de células madre embrionarias tenían propiedades semejantes a las células auténticas. Sin embargo, existe el mérito de seguir investigando el programa epigenético, la eficiencia de la recombinación meiótica y la precisión de la segregación cromosómica, y la capacidad de acumular transcritos maternos y orgánulos como las mitocondrias durante el crecimiento de los ovocitos. Tal investigación podría resultar potencialmente en una mayor eficiencia en la generación de ovocitos fertilizables que produzcan embarazos viables.
Traducir el trabajo de K. Hayashi sobre las células gonadales de ratón a seres humanos sería un desafío debido a las lagunas en nuestro conocimiento de la trayectoria de desarrollo de las células germinales humanas y las células somáticas de los ovarios. Además, la diferenciación de células germinales y la ovogénesis ocurren durante un período muy prolongado en humanos, lo que puede ser técnicamente difícil de recapitular in vitro. La historia de la traducción de desarrollos históricos del ratón al ser humano es notable por largos intervalos de tiempo: la derivación de las primeras células madre embrionarias humanas se retrasó 17 años con respecto a las células madre embrionarias de ratón. Es probable que la obtención de ovocitos humanos funcionales in vitro requiera paciencia y persistencia. No obstante, vale la pena perseguir este objetivo debido a los beneficios potenciales para las mujeres infértiles y el rescate de mamíferos en peligro de extinción.
Las investigaciones sobre la génesis de la ovogonía y los ovocitos humanos son un desafío debido a la inaccesibilidad de las gónadas, por lo que los modelos in vitro son esenciales para estudiar las primeras etapas del desarrollo y la ovogénesis de las células germinales. Por ejemplo, ¿qué gobierna el posicionamiento de los sitios de recombinación meiótica que posteriormente hacen que la meiosis femenina sea susceptible a la segregación cromosómica? Un modelo experimental proporcionaría una plataforma investigar la herencia epigenética y los efectos transgeneracionales vinculados a factores ambientales. La capacidad de generar una gran cantidad de ovocitos completamente desarrollados facilitaría los análisis bioquímicos y proteómicos para complementar los estudios basados en imágenes a los que los ovocitos se prestan tan maravillosamente.
Si la derivación in vitro de ovocitos humanos se vuelve factible, los ovocitos podrían usarse para tratar mujeres con insuficiencia ovárica causada por factores genéticos o ambientales o por intervenciones médicas como terapias contra el cáncer gonadotóxico, incluida la radiación gamma. Los ovocitos humanos también se utilizarían para tratar a mujeres que tienen dificultades para concebir debido a su avanzada edad reproductiva y para suministrar ovocitos de donantes como en la terapia de reemplazo mitocondrial. Sin embargo, cualquier uso clínico de ovocitos derivados de células madre embrionarias requeriría pruebas de seguridad muy estrictas y la consideración de las implicaciones éticas y legales.